Клинические поражения шейки матки
Содержание
- 1 Общие сведения
- 2 Причины предрака шейки матки
- 3 Классификация цервикального предрака
- 4 Симптомы предраковых заболеваний шейки матки
- 5 Диагностика предрака
- 6 Лечение предраковых заболеваний шейки матки
- 7 I. Экзо – и эндоцервициты
- 8 II. Истинная эрозия шейки матки
- 9 III. Лейкоплакия шейки матки
- 10 IV. Эндометриоз шейки матки
- 11 V. Предраковые заболевания шейки матки
- 12 VI. Рак шейки матки
- 13 Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Межевитинова Е.А., Абакарова П.Р., Хлебкова Ю.С.
- 14 Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Межевитинова Е.А., Абакарова П.Р., Хлебкова Ю.С.,
- 15 PRECANCEROUS CERVICAL LESIONS
- 16 Текст научной работы на тему «Предраковые поражения шейки матки тактика ведения»
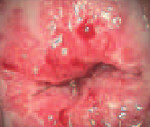
Предраковые заболевания шейки матки – ряд патологических состояний, которые при определенных условиях могут трансформироваться в рак шейки матки. К ним относятся дисплазия, лейкоплакия с атипией, эритроплакия, аденоматоз. У большинства женщин предраковые заболевания шейки матки протекают стерто; иногда могут сопровождаться водянистыми белями, контактными или межменструальными кровотечениями. Диагностируются на основании осмотра шейки матки в зеркалах, кольпоскопической картины, результатов онкоцитологии и биопсии, ВПЧ-типирования. В зависимости от характера и стадии предраковых изменений может осуществляться радиохирургическая, криогенная или лазерная деструкция патологического очага, конизация шейки матки или гистерэктомия.

Общие сведения
Предраковые заболевание шейки матки – диспластические процессы в области влагалищной части шейки матки с высоким риском малигнизации. В гинекологии различают фоновые заболевания шейки матки (псевдоэрозия и истинная эрозия, полипы, простая лейкоплакия, эндометриоз, эктропион, папилломы, цервициты) и предраковые. Для фоновых патологий характерна нормоплазия эпителиальных клеток – их правильное деление, созревание, дифференцировка, отторжение.
Отличительной особенностью предраковых заболеваний шейки матки является то, что они протекают с дисплазией эпителия – его гиперпластической трансформацией, пролиферацией, нарушением дифференцировки, созревания и эксфолиации. Тем не менее, в отличие от рака шейки матки, все эти клеточные изменения ограничены пределами базальной мембраны. В большинстве случаев предраковые процессы развиваются в области фоновых заболеваний и нередко маскируются ими, что затрудняет своевременную диагностику. Средний возраст пациенток с предраком шейки матки составляет 30-35 лет.

Причины предрака шейки матки
В настоящее время ключевой концепцией этиопатогенеза предраковых заболеваний шейки матки признана вирусная теория. Эпидемиологические исследования убедительно доказывают, что в развитии дисплазии ведущую роль играет папилломавирусная инфекция. В популяции женщин с тяжелой формой дисплазии шейки матки 85–95% являются ВПЧ-позитивными; у них, главным образом, обнаруживаются высокоонкогенные типы вируса — 16, 18 и 31. Попадая в организм при половых контактах, ВПЧ внедряется в клетки базального слоя эпителия. В инфицированной клетке вирус способен паразитировать в двух формах: доброкачественной, эписомальной и интрасомальной, стимулирующей опухолевый рост. Несмотря на то, что ВПЧ инфицирует базальные клетки, цитопатические эффекты возникают, в первую очередь, в клетках поверхностного слоя цервикального эпителия, где происходит вирусная репликация.
Возникновению предрака шейки матки способствует «содружество» ВПЧ, вируса простого герпеса II типа, хламидийной и цитомегаловирусной инфекций. Сочетание ВИЧ-инфекции и ВПЧ в разы повышает риск малигнизации. Важнейшим фактором, увеличивающим вероятность возникновения предраковых заболеваний шейки матки, является длительность персистенции вируса.
В меньшей степени, чем вирусные агенты, на риск развития фоновой и предраковой патологии шейки матки могут влиять и другие вероятные факторы риска. Так, ряд авторов ассоциирует цервикальную интраэпителиальную неоплазию (CIN) с курением. Доказано, что женщины, выкуривающие более 20 сигарет в день в течение 20 лет, имеют пятикратное повышение риска плоскоклеточной дисплазии. Содержащиеся в табачном дыме метаболиты проникают в цервикальную слизь и могут действовать и как самостоятельные канцерогены, и как факторы, активизирующие ВПЧ.
Установлена корреляция предраковых заболеваний шейки матки с длительным приемом эстроген-гестагенных оральных контрацептивов, особенно с повышенным гестагенным компонентом. Предраковыми заболеваниями шейки матки чаще страдают женщины, имеющие в анамнезе ранние роды, цервициты, травмы шейки матки при абортах и родах, нарушения гормональныго и иммунного гомеостаза. Среди других риск-факторов рассматриваются раннее (ранее 16 лет) начало половой жизни, частая смена половых партнеров, профессиональные вредности, отягощенный семейный анамнез по РШМ. Вместе с тем, ряд исследований показали, что длительный прием высоких доз витамина С и каротина может вызывать регресс интраэпителиальных цервикальных неоплазий.
Классификация цервикального предрака
Классификация предраковых заболеваний шейки матки претерпевала неоднократные пересмотры и уточнения. Одна из последних классификаций (1996 г.) выделяет доброкачественные фоновые изменения и собственно предрак. Согласно ей, к фоновым относятся дисгормональные (эктопия, эндометриоз, полипы), посттравматические (эктропион, рубцы, разрывы шейки матки), воспалительные (эрозия, цервицит) процессы.
Предраковые заболевания шейки матки, по данным кольпоцервикоскопического и гистологического исследования, делятся на несколько групп:
- Дисплазия (цервикальная интраэпителиальная неоплазия) — пролиферация атипического цервикального эпителия без изменения структуры стромального слоя и поверхностного эпителия. Включает в себя такие формы, как простая лейкоплакия, поля дисплазии, папиллярная и предопухолевая зона трансформации, предраковые полипы и кондиломы. Частота перерождения предрака шейки матки в рак колеблется в диапазоне 40-60%, зависит от вида патологии, ее локализации и длительности течения.
Различают легкую (CIN-I), умеренную (CIN-II) и тяжелую (CIN-III) дисплазию. При дисплазии легкой степени поражаются клетки глубоких — базального и парабазального – слоев (менее 1/3 толщины многослойного эпителия); атипичные клетки отсутствуют. Дисплазию умеренной степени характеризуют изменения 1/3-2/3 толщины эпителиального пласта; атипии не наблюдается. При тяжелой дисплазии на долю гиперплазированных клеток приходится более 2/3 толщи эпителиального слоя, встречаются клетки атипичной структуры.
- Лейкоплакия с атипией – морфологически характеризуется ороговением поверхностного эпителия, пролиферацией клеток базального слоя с явлениями атипизма, лимфоидной инфильтрацией подэпителиальной соединительной ткани. В 75% случаев дает начало инвазивному РШМ.
- Эритроплакия – предраковое заболевание шейки матки, протекающее с атрофией поверхностного и промежуточного слоем многослойного плоского эпителия; гиперплазией базального и парабазального слоев с наличием атипических клеток.
- Аденоматоз — атипическая гиперплазия желез эндоцервикса, напоминающая гиперплазию эндометрия. На фоне аденоматоза могут развиваться железистые формы рака.
Симптомы предраковых заболеваний шейки матки
Особенностью протекания предраковых заболеваний шейки матки является из бессимптомность или неспецифичность клинических проявлений. В основном данная группа патологий выявляется при проведении гинекологического осмотра и кольпоскопии с пробой Шиллера.
Дисплазия шейки матки не имеет самостоятельных симптомов. Лишь при присоединении вторичной инфекции может развиваться клиника вагинита или цервицита (бели, жжение, контактные кровянистые выделения). При изменениях, обусловленных гормональным дисбалансом, возможны нарушения менструльного цикла по типу мено- и метроррагий. Болевые ощущения отсутствуют.
Большинство женщин с лейкоплакией шейки матки считают себя практически здоровыми, лишь незначительная часть отмечает наличие обильных белей и контактных кровянистых выделений. Кольпоскопическая картина весьма патогномонична: участок лейкоплакии определяется в виде белесого перламутрового пятна. Дифференцировать простую и атипичную форму заболевания возможно только после гистологического изучения биоптата. Пациенток с эритроплакией могут беспокоить клейкие выделения желтоватого цвета. При кольпоскопии выявляются темно-красные участки с неровными границами, приподнятые над неизмененной слизистой.
Кондиломы шейки матки и аденоматозные полипы обнаруживаются, главным образом, при кольпоскопическом исследовании. При наличии в них вторичных изменений, вызванных изъязвлением, травматизацией и пр., возможно появление сукровичных выделений.
Диагностика предрака
Алгоритм диагностики предраковых заболеваний шейки матки разработан детально и включает в себя серию инструментальных и лабораторных исследований, позволяющих не только установить вид предрака, но и степень дисплазии.
При визуальном осмотре влагалищной порции шейки матки с помощью зеркал гинеколог оценивает форму наружного зева, окраску слизистой, характер секрета, видимые патологические процессы. В рамках гинекологического осмотра производится забор мазков с поверхности шейки матки для онкоцитологического исследования (ПАП-тест). При выявлении подозрительных участков шейки матки следующим этапом выполняется простая кольпоскопия, при необходимости – расширенное исследование с проведением медикаментозных проб (пробы Шиллера и др.). Каждой форме фоновых и предраковых заболеваний шейки матки соответствует своя кольпоскопическая картина, поэтому на данном этапе возможна дифференциальная диагностика патологий. Для выявления изменений эндоцервикса используется цервикоскопия.

Дальнейшая тактика обследования пациенток с подозрением на предраковые заболевания шейки матки предполагает осуществление прицельной биопсии шейки матки и выскабливания цервикального канала. На основании полученного гистологического заключения окончательно подтверждается или исключается предрак и определяется его форма. Дополнительная клинико-лабораторная диагностика может включать ПЦР исследование на ВПЧ с типированием, УЗИ малого таза, ОКТ шейки матки и др.
Лечение предраковых заболеваний шейки матки
Подход к лечению предраковых заболеваний шейки матки – дифференцированный и поэтапный. Целью терапии служит радикальное удаление патологически измененных тканей, устранение провоцирующих и сопутствующих факторов (лечение ВПЧ, иммунного и гормонального дисбаланса, воспалительных процессов). В соответствии с выявленными нарушениями назначается этиотропная противовоспалительная терапия (противовирусные, антибактериальные, иммуномодулирующие, интерферонстимулирующие, ферментные препараты). Проводится коррекция биоценоза влагалища, витаминотерапия, при необходимости – гормонотерапия.
Выбор способа хирургического лечения предраковых заболеваний шейки матки зависит от степени клеточной дисплазии. При CIN I-II, особенно у нерожавших пациенток, возможно щадящее физическое воздействие на патологические очаги: диатермокоагуляция, радиохирургическое лечение, лазерная вапоризация, криодеструкция. При CIN II-III показано радикальное хирургическое вмешательство в объеме эксцизии или конизации шейки матки, конусовидной ампутации или гистерэктомии (удаления матки). При полипах цервикального канала производится их удаление с РДВ.
После излечения предраковых заболеваний шейки матки контрольную кольпоцервикоскопию и онкоцитологию повторяют каждые 3 месяца на протяжении первого года и дважды в год в течение второго. Рецидивы редки, однако известно, что их процент выше у ВПЧ-инфицированных женщин. Профилактика предраковых заболеваний шейки матки предполагает широкий охват женского населения скрининговыми программами, вакцинацией против РШМ. Важную роль играет поведение самой женщины: использовании барьерной контрацепции при случайных контактах, отказ от курения, своевременное лечение фоновых заболеваний.
I. Экзо – и эндоцервициты
Это воспаление слизистой оболочки экзо – и эндоцервикса, причиной которого может быть как условно-патогенная микрофлора (стрептококки, стафилококки, кишечная палочка), так и урогенитальная инфекция (мико-, уреаплазмоз, трихомониаз, хламидиоз, вирусные инфекции).
Специфических клинических симптомов воспаления не существует, чаще всего заболевание проявляется появлением более обильных выделений из половых путей (бели), очень редко тупыми болями внизу живота, связанными в основном с сопутствующими заболеваниями (уретрит, цистит).
При гинекологическом осмотре обнаруживается гиперемия вокруг наружного зева, слизистые или гнойные выделения.
Кольпоскопия помогает не только диагностировать цервицит, но иногда и уточнить его этиологию.
Так по кольпоскопической картине можно дифференцировать воспаление хламидийной, вирусной, кандидозной и трихомонадной этиологии.
При трихоманадном цервиците , наблюдается так называемый симптом «земляничного цервикса», когда на шейки при кольпоскопии визуализируются мелкие петехиальные кровоизлияния.
Трихомонадный диффузный цервицит


Кандидозный цервицит сопровождается чередованием «шероховатых» зон с «лакированной» поверхностью, а так же появлением типичных творожистых выделений на шейки и стенках влагалища.

Типичным симптомом вирусного цервицита является симптом «большой эрозии», когда вся поверхность шейки матки ярко-красного цвета с изъявлениями.
Хламидийный цервицит сопровождается отеком эктопированого цилиндрического эпителия, очагами некроза и изъязвления, слизисто-гноевидными выделениями.
Для уточнения этиологии воспаления так же необходимо сдать мазок на флору, бак посев и чувствительность к антибиотикам из цервикального канала, соскоб на урогенитальную инфекцию методом ПЦР и РАР-тест для исключения фоновых и предраковых заболеваний.
Лечение зависит от возбудителя, вызвавшего воспаление и его чувствительности к антибиотикам.
Учитывая то, что чаще всего причиной являются несколько возбудителей, в лечении используют препараты местного действия, обладающие противовоспалительным, антибактериальным и противогрибковым эффектом (Полижинакс, Тержинан, Клион-Д, Бетадин).
При гонорейной, трихомонадной, герпетической этиологии цервицита в комплексе используют пероральные антибактериальные или противовирусные препараты.
II. Истинная эрозия шейки матки
Довольно часто врачи используют термин «эрозия шейки матки», тем самым обозначая, отклонения от нормы при осмотре невооруженным глазом. В основном эти «отклонения» оказываются обычной эктопией или псевдоэрозией.
 Истинная эрозия — это нарушение целостности эпителия (язва) и в репродуктивном периоде встречается редко.
Истинная эрозия — это нарушение целостности эпителия (язва) и в репродуктивном периоде встречается редко.
При этом происходит дистрофия и десквамация многослойного плоского эпителия с обнажением подэпителиальной стромы.
Причины истинной эрозии шейки матки.
1. Воспалительный процесс . Длительные выделения при кольпитах и цервицитах различной этиологии приводят к патологическим изменениям слизистой шейки матки, повышению проницаемости эпителия для микроорганизмов, его дистрофии и десквамации.
2. Травмы шейки матки . Механические повреждения шейки матки в родах и патологическая реакция на шовный материал, используемый для реконструкции разрывов, травматизация шейки матки зеркалами при осмотре могут быть одной из причин появления истинной эрозии шейки матки.
3. Ожоги шейки матки . После лечения шейки матки различными методиками (химио-, электро-, криодестукция), как правило, происходит отторжения струпа, в результате чего образуется эрозивная поверхность, которая постепенно эпителизируется.
4. Трофические нарушения . Группой риска для возникновения этого заболевания является пациентки с выпадением матки, когда ткани трамируются о белье, а также пациентки после лучевой терапии.
5. Гормональный дисбаланс . Немалую роль в появлении истинной эрозий играет дефицит женских половых гормонов в постменопаузе. Недостаток эстрагенов приводит к истончению слизистой, снижению секреции желез, сухости и, как следствие, ткани становятся более ранимыми.
6. Другие причины . Нарушения иммунитета, аллергические реакции, авитаминозы и нехватка минеральных веществ также могут способствовать появлению эрозии.
При кольпоскопии истинная эрозия выглядит, как дефект эпителия с четкими краями и неровным, бугристым дном.
В норме, если исключить воспалительный процесс поддерживающий эрозию, через 1-2 недели она начинает эпителизироваться.
Поэтому основным методом лечения, как истинной эрозии, является устранение воспалительного компонента. При лечении истинной эрозии шейки в постменопаузе используют комбинированное лечение, включающее исключение травмирующего фактора, противоспалительную и гормональную терапию.
Не стоит забывать о цитологическом исследовании шейки матки перед лечением, для исключения более серьезной патологии.
III. Лейкоплакия шейки матки
 Это поражение слизистой экзоцервикса, заключающееся в утолщении слизистой и нарушении процессов её ороговения, при этом на поверхности шейки матки образуются белые пленки или бляшки, плоские или возвышающиеся над поверхностью.
Это поражение слизистой экзоцервикса, заключающееся в утолщении слизистой и нарушении процессов её ороговения, при этом на поверхности шейки матки образуются белые пленки или бляшки, плоские или возвышающиеся над поверхностью.
При кольпоскопии выделяют три формы лейкоплакии шейки матки:
- плоская лейкоплакия – белесоватые участки находятся на одном уровне с нормальным многослойным плоским эпителием;
- бородавчатая лейкоплакия – поверхность шейки матки выглядит бугристой за счет наслоения пораженных участков друг на друга и возвышения их над поверхностью;
- эрозивная лейкоплакия – при кольпоскопии помимо лейкоплакии на шейке матки в пораженной зоне определяются эрозивные участки или трещины.
По гистологическому заключению выделяют простую лейкоплакию шейки матки (или без атипии) и лейкоплакию с атипией .
Простая лейкоплакия характеризуется утолщением базального и зернистого слоя многослойного плоского эпителия и явлениями паракератоза.
Причина этого процесса до конца не выяснена, но среди возможных причин выделяют нарушение гормонального фона женщины, травмы шейки матки, инфекционные и химические факторы.
Лейкоплакия с атипией относится к предраковым заболеваниям и заключается в появление базально-клеточной гиперактивности и атипичных клеток. В 15-75% случаев она может переходить в преинвазивный плоскоклеточный рак.
Кольпоскопия в этом случае не позволяет точно дифференцировать заболевание.
Единственным методом диагностики является цитологическое, а лучше гистологическое исследование.
Для этого проводят РАР-тест или биопсию участка лейкоплакии.
При подтверждении простой лейкоплакии на гистологическом уровне, никакого лечения не требуется, кроме наблюдения и проведения РАР-теста раз в год.
При обнаружении атипичных клеток при гистологическом исследовании, методом лечения является радиоволновое «прижигание» лейкоплакии на шейке матке на 5-7 день менструального цикла, в запущенных случаях применяется конизация шейки матки.
Применение тампонов с облепиховым маслом, алоэ и шиповником не допустимо, т.к. провоцирует бурный рост злокачественных клеток!
IV. Эндометриоз шейки матки
По данным литературы почти в 20% случаев эндометриоз шейки матки является результатом диатермокоагуляции. Так же некоторые исследователи к причинам развития эндометриоза шейки матки относят пластические операции, аборты и роды. Предполагают, что эндометрий внедряется в поврежденную слизистую шейки матки, формируя очаги гетеротопии.
При локализации эндометриоза только на влагалищной части шейки матки, заболевание может протекать бессимптомно, либо сопровождаться появлением мажущих темно-коричневых выделений до и после менструации.
При внедрении эндометриоидных очагов в слизистую цервикального канала присоединяется болевой синдром, меняющий свою интенсивность в зависимости от фазы цикла.
При кольпоскопии очаги эндометриоза выглядят, как кисты красноватого цвета, размерами до 5 мм, а в дни менструации они увеличиваются в размере и становятся багрово-синюшными.
Также перед лечением необходимо провести биопсию очагов с гистологическим заключением, для исключения злокачественных процессов.
Радикальным методом лечения эндометриоза шейки матки, так же как и других форм этого заболевания, является хирургический. На 6-7 день цикла проводят лазерную или радиоволновую деструкцию очагов.
Рецидив заболевания после этого встречается крайне редко.
V. Предраковые заболевания шейки матки
Рак шейки матки по данным литературы занимает 3-е место среди злокачественных заболеваний репродуктивной системы у женщин. Ежегодно регистрируется до 500000 новых случаев рака шейки матки в мире.
Но рак возникает не молниеносно, проходят десятки лет, прежде чем предрак перейдет в злокачественный процесс. Его можно предотвратить, если вовремя диагностировать и пролечить предраковые изменения.
Сложность в диагностике заключается в том, что даже выраженный процесс протекает бессимптомно, поэтому так важно проходить обследование у гинеколога хотя бы раз в год.
Многие исследования доказывают, что формирование предраковых процессов начинается с инфицирования вирусом папилломы человека, который впоследствии нарушает структурное строение клеток, больше всего затрагивая ядра клеток.
По классификации Bethesda system их относят к LSIL (плоскоклеточные интраэпителиальные поражения низкой степени значимости).
Кондиломы возникают в результате папилломовирусной инфекции и представляют собой разрастания соединительной ткани, покрытой многослойным плоским эпителием.
Выделяют остроконечные и плоские кондиломы.
Плоские кондиломы в 10% случаев могут малигнизироваться в течение 2-х лет, они незаметны невооруженным глазом и диагностируются при расширенной кольпоскопии.
Лечение кондилом заключается в лазерной хирургии пораженных очагов с дальнейшей противовирусной и иммуномодулирующей терапией.
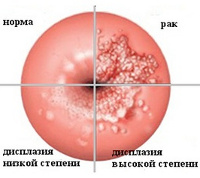
Дисплазия легкой степени (CIN I)

Изменения структуры клеток затрагивают только нижние слои многослойного плоского эпителия.
Как правило, эти изменения возникают вследствие воспалительного процесса и, либо проходят после противовоспалительной терапии, либо регрессируют сами.
В 10-15% случаев могут переходить в дисплазию средней степени.
Дисплазия средней степени (CIN II)

Характеризуются тем, что изменения в клетках затрагивают уже более высокие слои.
В 20% случаев переходит в CIN III, а в 5% может переходить в рак шейки матки.
Дисплазия тяжелой степени (CIN III) и рак in situ
 При CIN III изменения в клетках характеризуются появлением больших ядер или нескольких ядер на всех пластах слизистой. Лишь в самых поверхностных слоях можно обнаружить признаки созревания и дифференцировки нормальных клеток.
При CIN III изменения в клетках характеризуются появлением больших ядер или нескольких ядер на всех пластах слизистой. Лишь в самых поверхностных слоях можно обнаружить признаки созревания и дифференцировки нормальных клеток.
При раке in situ клетки по структуре не отличаются от раковых, но эти изменения ещё не вышли за пределы слизистой оболочки.
Учитывая то, что разные степени дисплазии могут сочетаться, для уточнения стадии и перед лечением необходимо проводить прицельную биопсию подозрительных участков с последующим гистологическим исследованием.
При CIN I-II лечение начинают с противовоспалительных препаратов с последующим повторным цитологическим исследованием через 2-е недели.
Также при обнаружении папилломовирусной инфекции в комплексе можно использовать противовирусную и иммуномодулирующую терапию.
Если при повторном исследовании изменения сохраняются, проводят лазерную коагуляцию шейки матки, как наиболее эффективный метод лечения.
Это амбулаторная процедура, проводимая на 4-7 день цикла. Полная эпителизация коагулированной поверхности наступает через 4-6 недель после процедуры.
В последующем необходимо динамическое наблюдение с цитологическим исследованием раз в 6 месяцев.
При CIN III и раке in situ выжидательная тактика неприемлема, необходимо сразу проводить конизацию шейки матки – ампутация шейки матки с последующим гистологическим исследованием материала.
Процедура проводится в стационаре под наркозом. При этом можно использовать различные методики: радиоволновая, лазерная, электрохирургическая или просто хирургическая.
Недостатком лазерной методики является то, что происходит обугливание краев материала, что затрудняет дальнейшую диагностику, но при этом риск развития кровотечения значительно ниже, чем после использования хирургического метода.
В последние годы широко применяют радиоволновой или аргоноплазменный метод с помощью специальной петли, который устраняет оба эти недостатка.
После проведения манипуляции также необходимо диспансерное наблюдение 1 р в 3 месяца.
VI. Рак шейки матки
Клинические симптомы появляются только на поздних стадиях, на ранних — заболевание протекает бессимптомно!
При этом все симптомы неспецифичны и могут быть признаком множества других гинекологических заболеваний.
Наиболее часто появляются жалобы на:
- Кровотечения после полового акта, осмотра гинеколога
- Кровянистые выделения в постменопаузе
- Изменение продолжительности и характера менструаций
- Боли или дискомфорт внизу живота
Поэтому диагностика рака шейки матки столь затруднительна. Основными методами ранней диагностики заболевания являются систематическое прохождение РАР-теста и кольпоскопии.
Лечение заключается в комплексном применении хирургических, лучевых и химиотерапевтических мероприятий.
Хирургическое лечение , в настоящее время, заключается в более щадящей, по сравнению с операцией Вертгейма-Мейгса, гистерэктомии – удалении матки с шейкой. Вопрос о придатках решают индивидуально, в зависимости от возраста и распространенности процесса.
В последние годы, все больше исследований доказывает более эффективное применение совместно лучевой и химиотерапии . Хотя такое лечение приводит к более тяжелым осложнениям и труднее переносится пациентками.
Прогноз при этом заболевании достаточно благоприятный. На ранних стадиях 5-ая выживаемость составляет более 90%, при второй-третьей стадии от 30 до 60%, а при четвертой около 10%.
- Консультация специалистом, акушером-гинекологом
- Расширенная кольпоскопия
- Онкоцитологическое обследование шейки матки
- Определение ВПЧ
- Хирургическое лечение с использованием радиоволновой или аргоноплазменной энергии
Аннотация научной статьи по медицине и здравоохранению, автор научной работы — Межевитинова Е.А., Абакарова П.Р., Хлебкова Ю.С.
Истинным предраковым состоянием являются неопластические изменения эпителия (цервикальные интраэпителиальные неоплазии , CIN). Причиной развития неопластических процессов считается вирус папилломы человека .
Похожие темы научных работ по медицине и здравоохранению , автор научной работы — Межевитинова Е.А., Абакарова П.Р., Хлебкова Ю.С.,
PRECANCEROUS CERVICAL LESIONS
Treatment approach Neoplastic epithelial changes (cervical intraepithelial neoplasia , CIN) can be precancerous. Human papillomavirus is considered to be the cause of neoplastic processes.
Текст научной работы на тему «Предраковые поражения шейки матки тактика ведения»
Е.А. МЕЖЕВИТИНОВА, д.м.н., П.Р. АБАКАРОВА, к.м.н., Ю.С. ХЛЕБКОВА
Научный центр акушерства, гинекологии и перинатологии им. академика В.И. Кулакова, Москва
ПРЕДРАКОВЫЕ ПОРАЖЕНИЯ ШЕИКИ МАТКИ
Истинным предраковым состоянием являются неопластические изменения эпителия (цервикальные интраэпителиальные неоплазии, CIN). Причиной развития неопластических процессов считается вирус папилломы человека.
Ключевые слова: предрак шейки матки, интраэпителиальные неоплазии, вирус папилломы человека, папиллома-вирусная инфекция.
E.A. MEZHEVITINOVA, MD, P.R. ABAKAROVA, PhD in medicine, Y.S. KHLEBKOVA
Scientific center for obstetrics, gynecology and perinatology named after V.I. Kulakov, Moscow
PRECANCEROUS CERVICAL LESIONS. Treatment approach
Neoplastic epithelial changes (cervical intraepithelial neoplasia, CIN) can be precancerous. Human papillomavirus is considered to be the cause of neoplastic processes.
Keywords: precancerous conditions of the cervix, intraepithelial neoplasia, human papillomavirus, papillomavirus infection.
CIN ХАРАКТЕРИЗУЕТСЯ НАРУШЕНИЯМИ В СТРОЕНИИ КЛЕТОК И СЛОЕВ ПЛОСКОГО ЭПИТЕЛИЯ. ИЗМЕНЕННЫЕ ЭПИТЕЛИАЛЬНЫЕ КЛЕТКИ СТАНОВЯТСЯ АТИПИЧНЫМИ — КРУПНЫМИ, БЕСФОРМЕННЫМИ, С МНОЖЕСТВЕННЫМИ ЯДРАМИ И ИСЧЕЗНОВЕНИЕМ РАЗДЕЛЕНИЯ ЭПИТЕЛИЯ НА СЛОИ. МКБ-Х — ДИСПЛАЗИИ ШЕЙКИ МАТКИ N 87. 0-9
ПЛОСКОКЛЕТОЧНЫЕ ИНТРАЭПИТЕЛИАЛЬНЫЕ ПОРАЖЕНИЯ
Цервикальная интраэпителиальная неоплазия
Доказано, что заболевания шейки матки, в т. ч. рак шейки матки, ассоциированы с вирусом папилломы человека (ВПЧ). Именно длительная персистенция ВПЧ в тканях органов нижнего отдела генитального тракта провоцирует развитие предраковых и раковых процессов шейки матки. Раннее выявление изменений эпителия, обусловленных ВПЧ, для предотвращения развития предрака и рака шейки матки осуществляется с помощью скрининга (основные методы -цитологическое исследование и ВПЧ-тест).
Предрак шейки матки Клиническая картина. CIN шейки матки и преинвазивная карцинома не имеют характерной клинической картины, как правило, протекают бессимптомно. Жалобы обусловлены сопутствующей гинекологической патологией. Выявление CIN — сложный процесс, т. к. она может располагаться на визуально не измененной шейке матки или сочетаться с фоновыми процессами. Четкой связи обнаружения CIN с макроскопическими изменениями шейки матки, такими как, например, эктопия, не существует. Чаще отмечается сочетание CIN с лейкоплакией шейки
матки, а также с плоскими и инвертированными кондиломами. Диагностика. Диагноз предракового состояния ставится при проведении комплексного обследования: цитологического, кольпоскопического, биопсии, выскабливания цервикаль-
ного канала с последующим гистологическим исследованием. Основным методом диагностики предраковых состояний шейки матки является гистологическое исследование патологически измененных участков шейки матки.
Предраковые процессы и зона трансформации
Кольпоскопическое исследование дает возможность выявить изменения, позволяющие отличить норму от патологии и тяжелую патологию от легкой; причем тяжелую дисплазию легче отличить от легкой, чем легкую дисплазию от нормы. Кроме того, одна кольпоскопическая картина может по-разному трактоваться разными врачами, это зависит от их квалификации.
Нормальная зона трансформации отличается от ненормальной наличием ацетобелого эпителия, кровенос-
ных сосудов и их реакцией на обработку шейки матки раствором уксусной кислоты. Для проявления ацетобелого эпителия раствор 3-5%-ной уксусной кислоты должен подействовать, поэтому необходимо наблюдение в течение 1-2 мин. Чем быстрее проявляется ацетобелый эпителий и чем более он плотный, тем тяжелее патология. Степень изменения ацето-белых участков — единственный критерий, статистически связанный со степенью тяжести процесса. Наиболее тяжелые поражения чаще всего выявляются в зоне перехода многослойного плоского эпителия в
цилиндрический. Зона ацетобелого эпителия после обработки 0,5%-ным раствором йода всегда йод-негативна и имеет четкие контуры
Кольпоскопия и межкапиллярные расстояния
Вовлеченные в диспластический процесс сосуды формируют своеобразную сетку в виде плиточной мозаики и образуют пространства, окруженные сосудами. Эти пространства могут быть большими или маленькими, округлыми или многоугольными, одинаковой или разной формы.
Кольпоскопия и сосудистый рисунок
В очаге CIN сосуды не сливаются между собой. Метапластический эпителий полностью заполняет складки цилиндрического эпителия. По мере пролиферации многослойного плоского эпителия участки цилиндрического эпителия и его сосуды сдавливаются. Расстояние между капиллярами увеличивается, питание эпителия нарушается. Дальнейшая пролиферация невозможна без развития васкуляризации. Наступает биологическое равновесие, и поэтому даже при отсутствии лечения CIN 3 может существовать несколько лет. Опухоль стимулирует рост капилляров, что, в свою очередь, обеспечивает ее метаболические потребности и возможность дальнейшего роста. Атипические сосуды не ветвятся.
КОЛЬПОСКОПИЯ И МЕЖКАПИЛЛЯРНЫЕ РАССТОЯНИЯ
— Сосуды могут быть нежными и слегка извитыми или грубыми и сильно извитыми
— При CIN 1 изменения могут не визуализироваться или появляться нежной мозаикой с одинаковыми по форме межсосудистыми участками
CIN 2 и CIN 3 представляют собой мозаику с грубыми разнокалиберными сосудами и разными по форме межсосудистыми участками Пунктация (нежная и грубая) и мозаика (нежная и грубая) обусловлены некоторыми интраэпителиальными изменениями без малигнизации
КЗ w« яг* 4 г T’Tvi-‘
Пунктация при CIN 1 и CIN 2
АТИПИЧЕСКИЕ СОСУДЫ ПРИ РАКОВОМ ПОРАЖЕНИИ ШЕЙКИ МАТКИ
ШТОПОРООБРАЗНЫЕ СОСУДЫ ПРИ ПЛОСКОКЛЕТОЧНОМ РАКЕ
Предраковые процессы и кольпоскопическая картина
Главная задача врача при проведении кольпоскопии -выявить участки измененного эпителия, взять биопсию из очагов, где предполагается CIN 2-3 или инвазивный рак и определиться в необходимости выскабливания цервикального канала.
Еще недавно существовало противоречие по нескольким аспектам диагностики и ведения цервикальной интраэпителиальной неоплазии. Вопрос о необходимости хирургического лечения при CIN 3 не ставился. Активно обсуждался вопрос о возможности консервативного лечения женщин с CIN 2 и тактике ведения женщин при CIN 1. В структуре цервикальной патологии граница между предраковыми и доброкачественными поражениями может быть проведена между CIN 1 и CIN 2-3.
В классификации Бетесда, разработанной в 1988 г., выделяют плоскоклеточные интраэпителиальные поражения низкой и высокой степени (squamous intraepithelial Lesions low and highgrade — L-SIL и H-SIL) и инвазивный рак. Плоскоклеточные интраэпителиальные поражения низкой степени включают изменения, связанные с папиллома-вирусной инфекцией (ПВИ) и слабой диспла-зией (CIN 1), а высокой степени — умеренную дисплазию (CIN 2), тяжелую дисплазию (CIN 3) и внутриэпителиаль-ный рак.
Поражения легкой степени (L-SIL)
Подавляющее большинство L-SIL развивается на фоне инфицирования высокоонкогенными типами ВПЧ, чаще всего ВПЧ 16. Большинство женщин с L-SIL инфицированы более чем одним типом ВПЧ. На ранних стадиях своего развития L-SIL является обратимым заболеванием, у большей части женщин (91%) может произойти регресс в течение последующих 3 лет. CIN 1 чаще всего представляет собой проявление продуктивной вирусной инфекции, обладает низким злокачественным потенциалом и редко требует лечения. Риск CIN 2 или более тяжелых изменений невелик и составляет примерно 28%. Рекомендовано консервативное лечение и контроль цитологического мазка 1 раз в 6 мес. или/и ДНК ВПЧ 1 раз в год. При трижды отрицательных результатах проводится стандартный скрининг.
Антибактериальные средства назначаются местно, парентерально и перорально. Обязательна коррекция нарушенного биоценоза влагалища при проведении антибактериальной терапии. С этой целью назначаются эубиотики (бактериальные биологические препараты), содержащие живые культуры микроорганизмов из флоры человека, например бифи-добактерии бифидум, лактобактерии ацидофильные и др. Течение ПВИ во многом зависит от состояния иммунной системы. В 70-80% случаев оно может быть транзитор-ным, и тогда наблюдается спонтанное очищение пораженной ткани от ВПЧ. Столь благоприятный исход возможен у молодых женщин с нормальным состоянием иммунной системы. В 20-30% случаев при ВПЧ-инфекции наблюдается прогрессирование заболевания. После элиминации вируса у части женщин сохраняются субклинические проявления инфекции, которые могут переходить в клиническую фазу у женщин с нарушением иммунитета. Наиболее неблагоприятное течение — персистирующее. При этом ВПЧ «обманывает» иммунную систему макроорганизма, что позволяет ему длительно персистировать ввиду своих эволюционно приобретенных особенностей — репликационный цикл ограничен эпителием, нет виремии, цитолиза воспаления, имеется локальная иммуносупрессия за счет вирусных белков. Персистенция ПВИ — выявление одного и того же высоко-онкогенного типа ВПЧ (трехкратно) на протяжении длительного периода времени (3 года) опасна в отношении развития CIN. При нарушениях механизмов контроля пролиферации ВПЧ-инфекция переходит в субклиническую и клиническую стадию. Так как состояние иммунной системы во многом определяет характер течения ВПЧ-инфекции, для повышения эффективности лечения ВПЧ-ассоциированных заболеваний целесообразным является применение медикаментозной противовирусной и имму-номодулирующей терапии. Используются такие препараты, как Изопринозин, полисахариды побегов SoLanum tuberosum и др. Изопринозин обладает противовирусным, иммуномодулирующим действием и может использоваться как самостоятельный препарат при легкой степени CIN. Из местных комбинированных антибактериальных средств применяются вагинальные суппозитории, таблетки (метронидазол, тиоконазол, миконазола нитрат и др.).
ИЗОПРИНОЗИН ДЕЙСТВУЕТ В ТРЕХ НАПРАВЛЕНИЯХ:
2. ВОССТАНАВЛИВАЕТ ИММУНИТЕТ (восстанавливает функции лимфоцитов в условиях иммунодепрессии, повышает активность клеточного иммунитета, продукцию интерферона-гамма, иммуноглобулинов С, хемотаксис нейтрофилов, моноцитов, макрофагов)
1. ВОЗДЕЙСТВУЕТ НА ВИРУСЫ (подавляет репликацию вирусов путем ингибирования трансляции вирусных белков)
3. УСТРАНЯЕТ КЛИНИЧЕСКИЕ ПРОЯВЛЕНИЯ ПВИ (при рецидивирующих остроконечных кандиломах в качестве монотерапии)
Источник: Инструкция по медицинскому применению Изопринозина РУ П №015167/01 от 11.02.2010.
Для лечения и ликвидации CIN нет преимущественного метода консервативной терапии. Тщательный цитологический контроль и возможное последующее кольпоскопи-ческое наблюдение без активного лечения — предпочтительная тактика ведения пациенток с CIN 1. Но она не лишена некоторого риска, т. к.:
• существует возможность того, что имеется поражение тяжелой степени, которое не было правильно диагностировано;
• характерным является то, что поражения тяжелой степени могут развиваться в период наблюдения;
• невозможно проводить дальнейшее наблюдение. Активное ведение женщин с CIN 1 рекомендуется в следующих случаях:
• неудовлетворительная кольпоскопическая картина;
• длительность течения CIN 1 (>18 мес.);
• возраст старше 35 лет;
• невозможность дальнейшего наблюдения. Поражения тяжелой степени (H-SIL)
У 70-75% женщин с H-SIL при гистологическом исследовании диагностируется CIN 2-3 и у 1-4% — инвазивный рак. Если CIN 2-3 подтверждена биопсией, то имеется повышенный риск развития инвазивного рака и пациентка должна быть пролечена.
Рекомендована эксцизия следующими методами: холодный нож, лазерная конизация, петлевая электроэксцизия.
ПРИ СОБЛЮДЕНИИ ПОЛНОГО КУРСА ИЗОПРИНОЗИНА В 98% СЛУЧАЕВ ЭЛИМИНИРУЕТСЯ ВИРУС ПАПИЛЛОМЫ ЧЕЛОВЕКА (ВПЧ)
Источник: Кедрова А.П, Подистов Ю.И., Кузнецов В.В., Козаченко В.Л., Никогосян С. Гинекология, 2005, 7: 170-174.
Абляция применима только в тех случаях:
• когда зона трансформации визуализируется полностью;
• нет признаков атипии желез;
• нет признаков инвазивных поражений;
• нет расхождений между данными кольпоскопического, цитологического и гистологического исследований.
Когда эксцизия проводится с лечебной целью, необходимо приложить все усилия, чтобы удалить пораженный участок одним куском. Удаление ткани должно происходить на глубину более 6 мм. Гистологический отчет должен содержать информацию о размере образца и состоянии резецированных краев в отношении интраэпители-ального или инвазивного поражения. У женщин старше 50 лет с неполной эксцизией и CIN по краю эндоцервикса высока вероятность рецидива. В связи с этим необходимо проведение адекватного цитологического контроля за эндоцервиксом. Эпителизация шейки матки после конизации и эксцизии происходит в течение 2-3 мес. Возможные осложнения — ранние (кровотечения в момент операции, нарушения менструальной функции, цервициты) и поздние (стенозирование канала шейки матки, эндометриоз, рецидивы, укорочение шейки матки и цервикального канала с развитием хронических воспалительных процессов верхних отделов гениталий) требуют профилактики и лечения. В качестве восстановительного и противорецидивного лечения применяется инозин пра-нобекс (Изопринозин), имеющий противовирусное и иммуномодулирующее действие. Препарат назначается в дозе по 50 мг/кг/сутки, разделенной на 3-4 приема в течение 10 дней. Далее 10 дней перерыв, 2-3 курса.
Особенности диагностической и лечебной тактики ведения CIN у беременных (ASCCP, 2006):
• на ранних сроках беременности у женщин с гистологически подтвержденным диагнозом CIN 2-3 допустимо проведение кольпоскопичес-кого и цитологического исследования с интервалом каждые 12 нед.;
• биопсия или диагностическая экс-цизия рекомендуется только в том случае, когда возникает подозрение на инвазивный рак и только в условиях стационара (повышен риск кровотечения и прерывания беременности);
• повторное исследование рекомендуется через 6 нед. после родов;
• активное лечение беременной пациентки допустимо только при инвазивном раке.
ПРИ ПОЛНОМ КУРСЕ ИЗОПРИНОЗИН ПОЗВОЛЯЕТ УВЕЛИЧИТЬ ЭФФЕКТИВНОСТЬ ХИРУРГИЧЕСКОГО ЛЕЧЕНИЯ ТЯЖЕЛОЙ ДИСПЛАЗИИ ШЕЙКИ МАТКИ В 1,8 РАЗА ПО ДАННЫМ КОЛЬПОСКОПИИ
n = 50 p i Не можете найти то, что вам нужно? Попробуйте сервис подбора литературы.
По данным кольпоскопии
ПРИ СОБЛЮДЕНИИ ПОЛНОГО КУРСА ТЕРАПИИ ИЗОПРИНОЗИНА В 3 РАЗА УМЕНЬШАЕТСЯ ЧАСТОТА РЕЦИДИВОВ ЗАБОЛЕВАНИЙ, АССОЦИИРОВАННЫХ С ПВИ
Прилепская В.Н., Роговская С.И. Возможности Изопринозина в лечении хронических цервицитов и вагинитов // РМЖ 2007. Том 16. №3. С.14
ISPR-RU-00267-DOK На правах рекламы
Статья подготовлена при поддержке компании ООО «Тева».


