Hbv инфекция это
Содержание
- 1 HBV — инфекция, вызванная вирусом гепатита B
- 2 Содержание
- 3 Эпидемиология [ править | править код ]
- 4 Патогенез [ править | править код ]
- 5 Течение [ править | править код ]
- 6 Клиника [ править | править код ]
- 7 Диагностика [ править | править код ]
- 8 Лечение [ править | править код ]
- 9 Профилактика [ править | править код ]
Диагностика хронической HBV инфекции. Диагноз хронической HBV инфекции ставится на основании выявления в сыворотке крови HBsAg. Дальнейшее обследование проводится для выяснения необходимости противовирусной терапии. С этой целью исследуют сыворотку крови на HBeAg и HBV DNA. Диагностические маркеры хронической HBV инфекции и их интерпретация указаны в табл. 4.2.
Таблица 4.2. Диагностические маркеры хронической HBV инфекции.
| Репликативная фаза | HBsAg, HBeAg, HBV DNA, anti-HBc IgG |
| Не (низко) репликативная фаза | HBsAg, anti-HBe, anti-HBc IgG |
| Прекоровые мутанты (см. главу 3) | HBsAg, HBV DNA, anti-HBe, anti-HBc IgG |
Об активности патологического процесса можно судить по уровню аминотрансфераз сыворотки крови (АЛТ и АСТ), которые отражают степень повреждения печени. В связи с отсутствием прямой корреляции между степенью некровоспалительной активности в ткани печени и уровнем АЛТ и АСТ, а также для определения стадии заболевания проводится гистологическое исследование ткани печени, которую получают методом пункционной биопсии.
Морфологические признаки хронического гепатита В. В биоптатах печени обнаруживают дистрофию и некроз гепатоцитов, воспалительную клеточную инфильтрацию и фиброзные изменения в дольках и портальных трактах (табл.4.3). Очень характерна гидропическая дистрофия гепатоцитов (рис. 4.4), реже — крайняя ее форма – баллонная дистрофия. Некроз гепатоцитов имеет вид цитолитического (колликвационного) или “Ацидофильного” (коагуляционного). В последние годы приводятся данные об апоптозе (программированной смерти) гепатоцитов. Повреждение и деструкция гепатоцитов обусловлены действием иммунных механизмов при участии Т-лимфоцитов, продукты распада клеток, в свою очередь, захватываются макрофагами. Поэтому очаги некроза паренхимы, как правило, содержат лимфоидно-макрофагальный инфильтрат (некро-воспалительная активность). Клетки инфильтрата (лимфоциты, макрофаги; в небольшом количестве плазмоциты и нейтрофилы) постоянно локализуются в портальных трактах.

Рис. 4.4. Хронический вирусный гепатит B (биоптат печени, окраска г/э, х100). Фиброзные септы с нарушением долькового строения печени, формирующаяся ложная долька. Гидропическая дистрофия гепатоцитов
| Гистологический признак | Число баллов |
|---|---|
| Перипортальные некрозы и мостовидные некрозы | 0 –10 |
Таблица 4.5. Полуколичественная система учета степени фиброза печени при определении стадии хронического гепатита (по В.В. Серову, 1996)
| Степень фиброза | Признаки | Баллы |
|---|---|---|
| Отсутствует | Нормальные портальные тракты | |
| Слабый | Фиброз и расширение портальных трактов, перипортальный фиброз. | 1 |
| Умеренный | Перипортальный фиброз, порто-портальные септы | 2 |
| Тяжелый | Порто-центральные септы, фиброз с нарушением долькового строения печени | 3 |
| Цирроз | Сформированный цирроз | 4 |
Хроническая HBV инфекция и алкоголь. Распространенность HBV инфекции среди алкоголиков в 2 – 4 раза выше, чем в общей популяции. Алкоголизм в сочетании с HBV инфекцией приводит к более тяжелому повреждению печени и способствует развитию цирроза и гепатоцеллюлярной карциномы. Продолжительность жизни неинфицированных алкоголиков выше, чем инфицированных. Однако, окончательно не известно, являются ли алкоголь и HBV независимыми повреждающими печень факторами, или действуют синергично.
Сочетание HBV с HCV или HDV. У 10 – 15% больных с ХГВ, циррозом печени или ГЦК выявляется HCV. Коинфекция HCV может удлинить инкубационный период заболевания, уменьшить срок HBsAg-емии, уменьшить пиковое значение сывороточных трансаминаз в сравнении с моноинфекцией HBV. В то же время, имеются данные о том, что острая коинфекция HCV и HBV может протекать в форме фульминантного гепатита.
Суперинфекция HCV у носителей HBsAg снижает уровень HBV DNA в сыворотке крови и ткани печени и повышает скорость сероконверсии HBsAg в anti-HBs. У большинства пациентов с двойной инфекцией (HBV и HCV)в сыворотке крови можно выявить HCV RNA, а не HBV DNA, что свидетельствует о способности вируса гепатита С подавлять репликацию HBV и определять течение болезни. Поражение печени у лиц с двойной инфекцией обычно тяжелее, чем при моноинфекции вирусом гепатита В. У этих больных чаще, чем при инфицировании одним вирусом, развивается ГЦК.
Острая коинфекция HBV и HDV протекает более тяжело, чем моноинфекция HBV и чаще приводит к фульминантному течению гепатита. Суперинфекция HDV у пациентов с хронической HBV инфекцией обычно сопровождается прекращением (супрессией) репликации HBV. Большинство исследователей полагают, что HDV суперинфекция приводит к более тяжелому повреждению печени и прогрессированию в цирроз, другие авторы это мнение не разделяют.
HBV инфекция и ГЦК. Повсеместно ГЦК занимает третье место по смертности от онкологических заболеваний среди мужчин и седьмое место среди женщин. Чаще всего эта форма рака встречается в эндемичных для HBV зонах.
HBV — инфекция, вызванная вирусом гепатита B
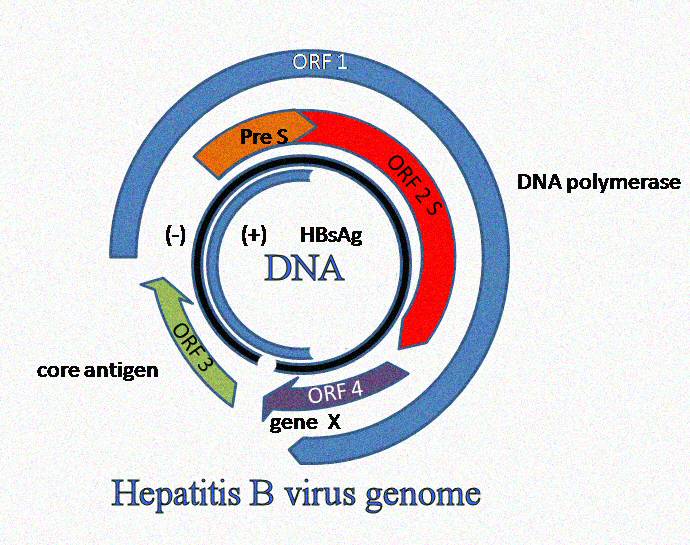 Как известно, при хронической вирусной инфекции для персистирования вирусы используют различные механизмы, среди которых наиболее важными являются нецитопатический способ репликации в клетках организма хозяина и возможность формирования латентного состояния, позволяющего вирусу избегать иммунного надзора . В последние годы благодаря достижениям молекулярной биологии латентная вирусная инфекция привлекает все большее внимание. Классическим примером латентной инфекции является вирус простого герпеса, который, как установлено, может длительное время сохраняться в клетках нервной системы, не экспрессируя свои антигены, что делает его недоступным для иммунной системы . В настоящее время возможность формирования латентной инфекции установлена и для вируса гепатита В (HBV). Клинико-биологическое значение и механизмы формирования латентной HBV инфекции, а также трудности ее диагностики изучаются в настоящее время достаточно интенсивно и являются предметом дискуссий. В данном обзоре мы попытались представить современное состояние этой проблемы.
Как известно, при хронической вирусной инфекции для персистирования вирусы используют различные механизмы, среди которых наиболее важными являются нецитопатический способ репликации в клетках организма хозяина и возможность формирования латентного состояния, позволяющего вирусу избегать иммунного надзора . В последние годы благодаря достижениям молекулярной биологии латентная вирусная инфекция привлекает все большее внимание. Классическим примером латентной инфекции является вирус простого герпеса, который, как установлено, может длительное время сохраняться в клетках нервной системы, не экспрессируя свои антигены, что делает его недоступным для иммунной системы . В настоящее время возможность формирования латентной инфекции установлена и для вируса гепатита В (HBV). Клинико-биологическое значение и механизмы формирования латентной HBV инфекции, а также трудности ее диагностики изучаются в настоящее время достаточно интенсивно и являются предметом дискуссий. В данном обзоре мы попытались представить современное состояние этой проблемы.
До настоящего времени хроническая HBV инфекция определялась как наличие в сыворотке крови поверхностного антигена HBV (HBsAg) в течение более 6 мес. после инфицирования, при этом термин «хроническая инфекция» включает в себя различные варианты сосуществования микро- и макроорганизмов. При HBV инфекции спектр и выраженность клинических проявлений зависят от взаимоотношений вируса и иммунной системы хозяина, варьируя от бессимптомного носительства вируса до тяжелого поражения различных органов и систем, прежде всего печени, но при всех формах хронической HBV инфекции обязательным ее условием являлось наличие в сыворотке крови HBsAg. Исчезновение HBsAg и появление антител к нему рассматривалось как признак освобождения организма от вируса, т.е. прекращения инфекции.
Однако в последние годы установлено, что у ряда больных, несмотря на отсутствие HBs-антигенемии и наличие anti-HBs, в ткани печени и сыворотке крови может обнаруживаться ДНК вируса (HBV DNA). При этом в сыворотке либо выявляли маркеры перенесенной HBV инфекции (антитела к антигенам вируса, прежде всего «изолированные» anti-HBc), которые, как теперь считают, могут быть признаком хронической латентной HBV инфекции, либо имело место отсутствие всех маркеров HBV (серонегативная инфекция). Клинико-морфологические исследования более ранних лет свидетельствовали об идентичности активности и стадии печеночного процесса у больных хроническими заболеваниями печени с наличием «изолированных» anti-HBc и у больных с HBs-антигенемией. Отсутствие сывороточных маркеров персистирования вирусной инфекции (HBsAg и/или HBeAg) при сохранении вируса в организме объясняют двумя основными причинами: очень низкой репликативной активностью вируса, вследствие чего экспрессия вирусных антигенов значительно подавлена; и наличием мутаций в геноме вируса, ведущих к нарушению синтеза вирусных антигенов, а также изменению их структуры, прежде всего HBsAg (HBsAg-мутантный штамм), что препятствует выявлению антигенов в крови доступными тест-системами. Механизмы развития низкоуровневой репликации HBV остаются неизученными, хотя известно, что суперинфекция вирусом гепатита D и/или С может оказывать ингибирующее влияние на репликацию HBV, что приводит к снижению уровня виремии HBV и клиренсу HBeAg, а в случае с HCV клиренсу не только HBeAg, но и HBsAg. Также отмечено, что алкоголь может вмешиваться в механизмы репликации вируса, и у лиц, злоупотребляющих алкоголем, часто единственным маркером хронической HBV инфекции являются anti-HBc. Аналогичное влияние на HBV характерно, в ряде случаев, и для вируса иммунодефицита человека (HIV). Так, в одном из исследований у 43% HIV-инфицированных в крови выявлялись anti-HBc, как единственный маркер сопутствующей HBV инфекции, при этом у 90% из них в сыворотке определялась HBV DNA.
В отсутствие других факторов большое значение в формировании низкоуровневой репликации HBV отводят мутациям в различных участках генома вируса, прежде всего в области перекреста С и Х генов, ответственных за репликацию вируса.
В связи с этим возникает вопрос о роли латентной HBV инфекции в развитии хронических диффузных поражений печени. Ряд авторов отмечают, что наличие латентной HBV инфекции у больных хроническим гепатитом С связано с более тяжелым течением болезни и низким ответом на противовирусную терапию. Улиц с алкогольным поражением печени наличие «изолированных» anti-HBc обусловливает неблагоприятный прогноз вследствие повышенного риска развития цирроза печени и гепатоцеллюлярной карциномы.
Несомненным фактом является то, что больные латентной HBV инфекцией могут быть источниками вируса и отвечать за развитие посттрансфузионного гепатита и инфицирование реципиентов донорских органов, особенно печени. Так, отмечены случаи, когда переливание крови и трансплантация органов от anti-HBc/anti-HBs позитивных доноров приводит к инфицированию реципиентов. Это связано с тем, что скрининг на HBV основывается на выявлении HBsAg, который не обнаруживается в случаях латентной инфекции, а также с тем, что обычные методы ПЦР не способны выявлять низкий уровень виремии. Широко обсуждается роль латентной HBV инфекции в развитии цирроза печени и гепатоцеллюлярной карциномы. Установлено, что, несмотря на клиренс HBsAg, возможно прогрессирование болезни вплоть до гепатоцеллюлярной карциномы. Если развитие гепатоцеллюлярной карциномы объясняют интеграцией генома вируса в геном клеток печени с последующей активацией про-онкогенов и подавлением опухоль-супрессорных генов, главным образом р53 (один из возможных механизмов развития рака печени), то патогенез повреждений печени при латентной вирусной инфекции остается неясным. В ряде исследований у больных с поражением печени неизвестной этиологии, имеющих признаки умеренной и высокой активности воспалительного процесса и далеко зашедшего фиброза в отсутствие серологических маркеров HBV инфекции, при использовании высокочувствительных методов ПЦР — «nested» PCR — в сыворотке выявлялась HBV DNA, а при иммунногистохимическом исследовании в ткани печени — антигены HBV. Это позволяет обсуждать роль латентной HBV инфекции в развитии криптогенных поражений печени, хотя сами авторы не исключают этиологическое значение еще неизвестных гепатотропных вирусов.
Известно, что длительная иммунносупрессивная терапия (химиотерапия опухолей, лечение аутоиммунных заболеваний, профилактика реакции отторжения трансплантата), прежде всего применение глюкокортикостероидов, может привести к реактивации латентной HBV инфекции, вплоть до развития фульминантного гепатита с летальным исходом. В патогенезе реактивации латентной HBV инфекции на фоне иммунносупрессивной терапии основное значение придают действию глюкокортикостероидов. Так, известно, что геном HBV содержит глюкокортикоид-чувствительные участки, активация которых усиливает репликацию вируса, продукцию и экспрессию вирусных антигенов на поверхности гепатоцитов. При этом поражение печени в ходе терапии глюкокортикостероидами обусловлено прямым цитопатическим действием вируса — усиленный синтез вирусных антигенов, прежде всего HBsAg, приводит к их избыточному накоплению в цитоплазме клеток печени, с последующей дистрофией, некрозом гепатоцитов и развитием тяжелого холестатического поражения печени. В качестве примера можно привести особую клиническую форму хронического гепатита В — фиброзирующий холестатический гепатит, развивающийся у лиц, которым после трансплантации печени длительно проводят иммунносупрессивную терапию глюкокортикостероидами. Эта форма хронического гепатита В по своим клинико-морфологическим признакам похожа на поражение печени при дефиците а l-антитрипсина, что, по-видимому, связано с общностью генеза поражения гепатоцитов: в первом случае в клетке накапливается HBsAg, во втором а l-антитрипсин. Поражение печени возможно и при резкой отмене глюкокортикостероидов, когда на фоне прекращения иммунносупрессивного действия глюкокортикостероидов и в ответ на повышенную экспрессию вирусных антигенов на поверхности гепатоцитов, прежде всего HBcAg, происходит иммунноопосредованный цитолиз гепатоцитов цитотоксическими лимфоцитами — так называемый синдром «рикошета».
«HBsAg-мутантная» инфекция (при которой в крови циркулирует структурно-измененный поверхностный антиген) представляет серьезную опасность для населения. Во-первых, она является потенциальным источником заражения реципиентов крови и донорских органов, так как во многих странах мира HBsAg является основным и единственным скрининговым маркером HBV-инфекции. Во-вторых, «HBsAg-мутантный» штамм является серьезной проблемой для программ вакцинации, так как вакцин-индуцированные антитела не обеспечивают иммунитет от инфицирования HBsAg-мутантным штаммом («вакцин-ускользающий штамм»). У таких пациентов, несмотря на наличие в сыворотке anti-HBs, инфицирование такими штаммами может вызвать гепатит В. Данный штамм может также привести к реинфицированию печени в посттрансплантационном периоде, несмотря на профилактику специфичным иммуноглобулином (HB Ig), который представляет собой поликлональные антитела к основным эпитопам поверхностного антигена HBV. Вследствие изменения структуры поверхностного антигена у HBsAg-мутантного штамма, антитела неспособны нейтрализовать вирус и предотвратить развитие инфекции.
Таким образом, анализ результатов исследований, посвященных этой проблеме, позволяет охарактеризовать латентную HBV инфекцию как гепатит В с наличием показателей репликации вируса (обнаружение HBV DNA в сыворотке крови и/или ткани печени) при отсутствии других серологических маркеров, указывающих на персистирование вируса (прежде всего негативный результат выявления HBsAg). Можно выделить два варианта латентной HBV инфекции. При первом, низкий уровень репликации HBV и, как следствие, пониженный синтез и экспрессия вирусных антигенов обусловлены влиянием ряда факторов: адекватного ответа иммунной системы; ингибирующего влияния на HBV других вирусов /HCV, HDV, HIV/; мутаций в определенных участках генома вируса, ответственных за его репликативную активность. При втором варианте репликация вируса не подавлена, HBsAg синтезируется и экспрессируется, но не выявляется современными коммерческими тест-системами вследствие мутаций, изменяющих структуру его основных детерминант.
В настоящее время можно считать установленными следующие факты, имеющие значение для клинической практики:
роль HBsAg как единственного и главного скринингового маркера хронической HBV инфекции требует пересмотра;
наличие anti-HBs не является абсолютным признаком освобождения организма от вируса;
больные с латентной HBV инфекцией могут быть источниками вируса при посттрансфузионном гепатите и поражении печени у реципиентов донорских органов. Определение HBsAg в службе переливания крови и в трансплантологии как единственного маркера наличия HBV не гарантирует полного исключения случаев гепатита В у реципиентов. Целесообразно применение тестов для выявления anti-HBc и тестирования DNA HBV, включая современные высокочувствительные варианты ее детекции;
латентная HBV инфекция может ухудшать течение хронических диффузных заболеваний печени, вызванных другими причинами, прежде всего алкоголем и HCV инфекцией, и связана с более плохим ответом на противовирусную терапию у последних;
длительная иммунносупрессивная терапия может привести к активации латентной инфекции с развитием тяжелого поражения печени вплоть до фульминантного гепатита; поэтому перед началом такой терапии необходимо тщательное вирусологическое обследование, а при выявлении латентной HBV инфекции, необходим постоянный мониторинг уровня виремии (количественное определение HBVDNA в сыворотке крови) и биохимических печеночных тестов в ходе и после лечения;
не исключается онкогенный потенциал латентной HBV инфекции; при ее наличии больные требуют длительного, возможно, пожизненного наблюдения на предмет выявления гепатоцеллюлярной карциномы (динамический УЗИ-контроль и определение уровня альфа-фетопротеина);
у больных криптогенным гепатитом, имеющих латентную HBV инфекцию и признаки активного поражения печени (по данным биохимического и морфологического исследований), может обсуждаться применение противовирусной терапии;
актуальной проблемой современной медицинской науки являются исследования по усовершенствованию существующих вакцин для профилактики вирусного гепатита В и тест-систем для выявления HBsAg.
До настоящего времени остаются неясными патогенетические механизмы развития поражений печени при латентной HBV инфекции. Каким образом столь низкая репликативная активность вируса может вызывать воспалительные изменения в печени? Служит ли выявление латентной HBV инфекции у больных с криптогенными заболеваниями печени доказательством ее этиологической роли или она лишь фон, пусть и неблагоприятный, на котором реализует свое действие какой-либо еще неизвестный агент? Кроме того, требует своего изучения и возможная триггерная роль латентной HBV инфекции в развитии аутоиммунного гепатита, при котором могут выявляться антитела к HBV, в том числе «изолированные» anti-HBc.
Учитывая возросшее значение и роль латентной HBV инфекции в развитии поражений печени, весьма актуальной становится разработка доступных, воспроизводимых и чувствительных способов ее диагностики. Появление в широкой клинической практике диагностических препаратов, способных выявлять мутантные формы вируса гепатита В и его антигены, способствовало бы более углубленному изучению патогенетических механизмов формирования латентной HBV инфекции и ее роли в развитии болезней печени.
Д. Т. Абдурахманов, Кафедра терапии и профессиональных болезней ММА им. И. М. Сеченова
| Гепатит B | |
|---|---|
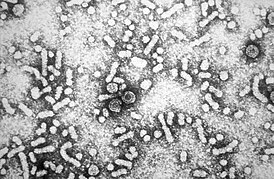 Электронная микрофотография вируса гепатита B |
|
| МКБ-11 | 1E50.1 1E50.1 , 1E51.0 1E51.0 , KA62.9 KA62.9 |
| МКБ-10 | B 16 16. , B 18.0 18.0 -B 18.1 18.1 |
| МКБ-9 | 070.2 070.2 — 070.3 070.3 |
| МКБ-9-КМ | 070.30 [1] |
| DiseasesDB | 5765 |
| MedlinePlus | 000279 |
| eMedicine | med/992 ped/978 ped/978 |
| MeSH | D006509 |
Гепати́т В — антропонозное вирусное заболевание, вызываемое возбудителем с выраженными гепатотропными свойствами — вирус гепатита B (в специальной литературе его могут обозначать «вирус ГВ», ВГВ или HBV) из семейства гепаднавирусов.
Поверхностный антиген гепатита B открыл в 1964 году американский врач и вирусолог Барух Самуэль Бламберг при изучении образцов крови австралийского аборигена, получивший в последующем за исследования гепатита B Нобелевскую премию по физиологии или медицине в 1976 году.
Вирус отличается чрезвычайно высокой устойчивостью к различным физическим и химическим факторам: низким и высоким температурам (в том числе кипячению), многократному замораживанию и оттаиванию, длительному воздействию кислой среды. Во внешней среде при комнатной температуре вирус гепатита B может сохраняться до нескольких недель: в пятнах крови, на лезвии бритвы, конце иглы. В сыворотке крови при температуре +30°С инфекционность вируса сохраняется в течение 6 месяцев, при температуре −20°С около 15 лет; в сухой плазме — 25 лет. Инактивируется при автоклавировании в течение 30 минут, стерилизации сухим жаром при температуре 160°С в течение 60 минут, прогревании при 60°С в течение 10 часов.
Содержание
Эпидемиология [ править | править код ]
Инфицирование вирусом гепатита B (HBV) остается глобальной проблемой здравоохранения, и, по оценкам, около 2 миллиардов людей во всем мире были инфицированы этим вирусом, более 350 миллионов людей больны.
Механизм передачи инфекции — парентеральный. Заражение происходит естественным (половой, вертикальный, бытовой) и искусственным (парентеральным) путями. Вирус присутствует в крови и различных биологических жидкостях — слюне, моче, сперме, влагалищном секрете, менструальной крови и др. Контагиозность (заразность) вируса гепатита B в 50-100 раз выше, чем у ВИЧ [2] [3] : инфицирующая доза составляет 0,0000001 мл сыворотки, содержащей ВГВ [4] .
Половой путь [ править | править код ]
В последние годы всё большее значение в развитых странах приобретает половой путь передачи вируса, что обусловлено, во-первых, снижением значения парентерального пути (появление разового инструментария, применение эффективных дезинфицирующих средств, ранним выявлением больных доноров), во-вторых, так называемой «сексуальной революцией»: частой сменой половых партнёров, практикованием анальных контактов, сопровождающихся бо́льшей травматизацией слизистых и, соответственно, возрастанием риска попадания вируса в кровоток. При этом инфицирование при поцелуях, передача инфекции через молоко матери, а также распространение воздушно-капельным путём считается невозможным [5] . Распространение наркомании также играет большую роль, поскольку «внутривенные» наркоманы входят в группу высокого риска и, что немаловажно, они не являются изолированной группой и с лёгкостью вступают в беспорядочные незащищённые половые отношения с другими людьми. Примерно 16-40 % половых партнёров при незащищённом половом контакте заражаются вирусом. [ источник не указан 3720 дней ]
Вертикальный путь [ править | править код ]
Большое значение в странах с интенсивной циркуляцией вируса (высокой заболеваемостью) имеет как трансплацентарый путь передачи, когда ребёнка заражает мать, так и контактный, когда заражение происходит во время родов при прохождении через родовые пути. Имеет большое значение активность инфекционного процесса в организме матери. Так, при положительном HBe-антигене, косвенно свидетельствующем о высокой активности процесса, риск инфицирования возрастает до 90 %, тогда как при единственном положительном HBs-антигене — такой риск составляет не более 20 %. [ источник не указан 3720 дней ]
Бытовой путь [ править | править код ]
При бытовом пути заражения инфицирование происходит в семье, ближайшем окружении и в организованных коллективах. Опасность представляют пользование общими бритвами, лезвиями, маникюрными и банными принадлежностями, зубными щётками, полотенцами и т. д. Опасными являются любые микротравмы кожи или слизистых оболочек предметами, а также соприкосновение с ними поврежденной поверхностью (потёртости, порезы, трещинки, воспаления кожи, проколы, ожоги и т. п.), на которых имеется даже малое количество инфицированных биологических жидкостей (крови, спермы, слюны).
Парентеральный путь [ править | править код ]
Парентеральный путь осуществляется через медицинский, лабораторный инструментарий и изделия медицинского назначения, контаминированные ВГВ. Заражение вирусным гепатитом B может происходить также при трансфузиях крови и/или её компонентов при наличии в них ВГВ.
В передаче вирусного гепатита B значительное место занимают немедицинские инвазивные процедуры в организациях бытового обслуживания (парикмахерских, маникюрных, педикюрных, косметологических), в кабинетах татуировки, пирсинга и прочих инвазивных процедур [4] .
С течением времени в России возрастная структура заболевших острым вирусным гепатитом B существенно меняется. Если в 70-80-х годах сывороточным гепатитом чаще болели 40-50-летние люди, то в последние годы от 70 до 80 % заболевших острым гепатитом B — молодые люди в возрасте 15-29 лет. [ источник не указан 3720 дней ]
Патогенез [ править | править код ]
Самый значимый патогенетический фактор при вирусном гепатите B — гибель заражённых гепатоцитов вследствие атаки собственными иммунными агентами. Массивная гибель гепатоцитов приводит к нарушению функций печени, прежде всего детоксикационной, в меньшей степени — синтетической.
Течение [ править | править код ]
Инкубационный период (время с момента заражения до появления симптомов) гепатита B составляет в среднем 12 недель, но может колебаться в пределах от 2 до 6 месяцев. Инфекционный процесс начинается с момента попадания вируса в кровь. После попадания вирусов в печень через кровь идёт скрытая фаза размножения и накопления вирусных частиц. При достижении определённой концентрации вируса в печени развивается острый гепатит B. Иногда острый гепатит проходит для человека практически незаметно, и обнаруживается случайно, иногда протекает в легкой безжелтушной форме — проявляется только недомоганием и снижением работоспособности. Исследователи полагают, что бессимптомное течение, безжелтушная форма и «желтушный» гепатит составляют равные по количеству поражённых лиц группы. То есть выявленные диагностированные случаи острого гепатита B составляют только одну треть всех случаев острого гепатита. По данным других исследователей на один «желтушный» случай острого гепатита B приходится от 5 до 10 случаев заболеваний, которые как правило не попадают в поле зрения врачей. Между тем представители всех трёх групп потенциально заразны для окружающих.
Острый гепатит либо постепенно сходит на нет с элиминацией вируса и оставлением стойкого иммунитета (функция печени восстанавливается через несколько месяцев, хотя остаточные явления могут сопровождать человека всю жизнь), либо переходит в хроническую форму.
Хронический гепатит B протекает волнообразно, с периодическими (иногда имеющими сезонный характер) обострениями. В специальной литературе этот процесс обычно описывают как фазу интеграции и репликации вируса. Постепенно (интенсивность зависит как от вируса, так и иммунной системы человека) гепатоциты заменяются на клетки стромы, развивается фиброз и цирроз печени. Иногда следствием хронической HBV-инфекции бывает первичноклеточный рак печени (гепатоцеллюлярная карцинома). Присоединение вируса гепатита D к инфекционному процессу резко меняет течение гепатита и увеличивает риск развития цирроза (как правило, у таких больных рак печени не успевает развиться).
Стоит обратить внимание на следующую закономерность: чем раньше человек заболевает, тем вероятность хронизации выше. Например, более 95 % взрослых людей заболевших острым гепатитом B, выздоравливают. А из заболевших гепатитом B новорожденных избавятся от вируса только 5 %. Из заразившихся детей в возрасте 1-6 лет хрониками станут около 35 %.
Клиника [ править | править код ]
Вся симптоматика вирусного гепатита B обусловлена интоксикацией вследствие снижения детоксикационной функции печени и холестазом — нарушением оттока желчи. Причём предполагается [ кем? ] , что у одной группы больных превалирует экзогенная интоксикация — от токсинов поступающих с сырой едой или образующихся при пищеварении в кишечнике, а у другой группы больных превалирует эндогенная — от токсинов, образующиеся в результате метаболизма в собственных клетках и при некрозе гепатоцитов.
Поскольку к любым токсинам чувствительна прежде всего нервная ткань, в частности нейроциты головного мозга, прежде всего наблюдается церебротоксический эффект, что приводит к повышенной утомляемости, нарушению сна (при лёгких формах острого и хроническом гепатите), и спутанности сознания вплоть до печёночной комы (при массивном некрозе гепатоцитов или последних стадиях цирроза печени) Не путаем причину со следствием? Нарушается функция печени — удаление токсинов — токсины поражают нервные клетки .
При поздних стадиях хронического гепатита, при обширном фиброзе и циррозе на первый план выступает синдром портальной гипертензии отягощённый хрупкостью сосудов вследствие снижения синтетической функции печени. Геморрагический синдром также характерен для фульминантного гепатита.
Иногда при гепатите B развивается полиартрит.
Диагностика [ править | править код ]
В России врачи всех специальностей, средние медицинские работники лечебно-профилактических учреждений независимо от форм собственности и ведомственной принадлежности, а также детских, подростковых и оздоровительных учреждений выявляют больных острыми и хроническими формами гепатита B, носителей ВГВ на основании клинико-эпидемиологических и лабораторных данных при оказании всех видов медицинской помощи. Проводится серологический скрининг групп людей с высоким риском заражения [4] .
При первичной диагностике основанной на клинических данных, невозможно отличить гепатит В от гепатита, вызываемого другими вирусными агентами, потому чрезвычайно важным является лабораторное подтверждение диагноза. Существует несколько видов анализа крови для диагностики и мониторинга людей с гепатитом В. Эти анализы можно использовать для того, чтобы отличить острую и хроническую инфекции [6] . Окончательный диагноз ставится после лабораторных исследований (показатели функции печени, признаки цитолиза, серологические маркеры, выделение ДНК вируса).
Диагностические маркеры HBV-инфекции [ править | править код ]
Для постановки диагноза следует выявлять серологические маркеры инфицирования вирусом гепатита B (HBsAg, анти-HBcIgM, анти-HBc, анти-HBs, HBeAg, анти-HBe) и ДНК вируса (HBV-DNA). В организме зараженных вирусом ГВ людей с разной частотой и на разных этапах могут быть выявлены поверхностный HBsAg, E-aнтиген-(HBeAg) и антитела к этим антигенам, а также вирусоспецифическая ДНК (HBV-DNA). [4]
Дифференциальная диагностика [ править | править код ]
Обычно вирусный гепатит B не представляет сложностей в правильной диагностике. Сложности возникают только при супер- и коинфекциях (когда сложно выделить активный на данный момент агент), а также при наличии неинфекционных заболеваний печени и желчевыводящих протоков.
Лечение [ править | править код ]
Острый гепатит B обычно не требует лечения, так как большинство взрослых справляются с этой инфекцией спонтанно [7] [8] . Раннее противовирусное лечение может потребоваться менее, чем 1 % заболевших: пациентам с агрессивным развитием инфекции (молниеносный гепатит) и лицам с ослабленным иммунитетом. С другой стороны, лечение хронической инфекции может быть полезным для уменьшения риска цирроза и рака печени. Хронически инфицированные лица с постоянно повышенным уровнем аланинаминотрансферазы, маркёра повреждения печени и большим количеством ДНК HBV, являются предпочтительными кандидатами для терапии [9] . Лечение длится от шести месяцев до года, в зависимости от препарата и генотипа вируса [10] .
Хотя ни один из имеющихся препаратов не способен полностью очистить организм пациента от вируса гепатита B, они могут остановить размножение вируса, тем самым сводя к минимуму повреждение печени. По состоянию на 2016 год существует восемь препаратов, лицензированных для лечения инфекционного гепатита В в Соединенных Штатах. К ним относятся:
противовирусные препараты прямого действия (ПППД):
Нуклеозиды ламивудин, телбивудин и нуклеотид адефовир морально устарели и не рекомендуются ввиду низкого порога резистентности и возможности формирования перекрёстной резистентности вируса к энтекавиру и препаратам тенофовира соответственно. [11] Всемирная организация здравоохранения рекомендовала в качестве терапии первой линии энтекавир либо тенофовир. [12] Приём энтекавира противопоказан при беременности; нефротоксичный и токсичный для костей ТДФ желательно, по возможности, заменить на ТАФ. Пациенты с циррозом в наибольшей степени нуждаются в лечении. Лечение препаратами прямого действия имеет умеренный уровень побочных эффектов, но симптоматическое, выражается в подавлении вирусной нагрузки — оно практически никогда не ведёт к сероконверсии вируса.
В отличие от терапии препаратами прямого действия, интерферонотерапия имеет высокий уровень побочных эффектов, однако выгодно отличается от терапии ПППД тем, что чаще приводит к сероконверсии HBeAg (маркёра репликации вируса). Ответ на лечение интерферонами зависит от нескольких факторов. Некоторые пациенты имеют гораздо больше шансов ответить на терапию, по сравнению с остальными. Причина может быть в генотипе вируса, которым заражён человек, а также в генетических особенностях самого пациента. Лечение снижает репликацию вируса в печени, тем самым снижая вирусную нагрузку (количество вирусных частиц в крови) [13] . Сероконверсия HBeAg при интерферонотерапии наблюдается у 37 % пациентов, поражённых HBV генотипа A, но всего лишь у 6 % пациентов, заражённых вирусом HBV генотипа D. Генотип HBV B имеет аналогичные типу А показатели сероконверсии HBeAg. В случае HBV генотипа C сероконверсия наблюдается только в 15 % случаев. Устойчивое снижение количества HBeAg после лечения составляет
45 % пациентов для типов А и В, 25-30 % пациентов для типов C и D [14] . Применение интерферона, требующего инъекций ежедневно или три раза в неделю, было вытеснено пэгилированным интерфероном — препаратом длительного действия, инъекции которого проводятся только один раз в неделю [15] .
Профилактика [ править | править код ]
Вакцинация [ править | править код ]
Вакцинация от гепатита B является универсальным способом защиты для всех путей заражения.
Вакцины для профилактики гепатита B в Соединённых Штатах широко рекомендуются для младенцев с 1991 года [16] . Первая доза обычно рекомендуется в течение первых суток после рождения [17] .
Большинство вакцин применяется в трёх дозах в течение нескольких месяцев. Защитный ответ на вакцину определяют как концентрацию антител против HBs по меньшей мере 10 мМЕ/мл в сыворотке крови. Вакцина более эффективна у детей: 95 % вакцинированных имеют защитные уровни антител. Их уровень снижается примерно до 90 % в возрасте 40 лет и примерно до 75 % у лиц старше 60 лет. Защита, обеспечиваемая вакцинацией, длится даже после того, как уровни антител опускаются ниже 10 мМЕ/мл.
Все, кто подвержен воздействию жидкостей организма, таких как кровь, должны быть вакцинированы [16] . Рекомендуется проводить тестирование для проверки эффективной иммунизации, а дополнительные дозы вакцины предоставляются тем, кто недостаточно иммунизирован [16] .
В исследованиях, которые продолжались от 10 до 22 лет, не было случаев гепатита B среди вакцинированных лиц с нормальной иммунной системой. Зарегистрированы только редкие хронические инфекции [18] . Вакцинация особенно рекомендуется для групп высокого риска, включая работников здравоохранения, людей с хронической почечной недостаточностью и мужчин, имеющих половые контакты с мужчинами [19] [20] [21] .
Руководящие указания в Великобритании гласят, что первоначально ответившие на прививку лица (получившие иммунитет благодаря прививкам) нуждаются в дальнейшей защите (это касается людей, находящихся в зоне риска заражением гепатитом B). Им рекомендуется, для сохранения иммунитета к вирусу гепатита B, повторная ревакцинация — раз в пять лет [22] .
Половой путь [ править | править код ]
Безопасный секс, включая сведение к минимуму числа партнёров и использование барьерных методов (презервативов), защищают от передачи инфекции [6] .
Вертикальный путь [ править | править код ]
Профилактика вертикальной передачи вируса гепатита B от инфицированной матери к ребёнку непосредственно во время беременности рекомендована, по крайней мере, женщинам с высокой вирусной нагрузкой и/или высоким уровнем HBsAg, начиная с 24-28-ой недель беременности и до 12 недель после родов.
Для тех новорожденных, чьи матери инфицированы HBsAg: только одна вакцина против гепатита В, только иммуноглобулин гепатита В или комбинация вакцины плюс иммуноглобулин против гепатита В [23] . Эти меры предотвращают передачу HBV во время родов в 86 % −99 % случаев [24] .
Для профилактики используется исключительно [ источник не указан 316 дней ] тенофовир: если беременная женщина уже принимает препараты прямого противовирусного действия (ПППД), отличные от тенофовира, то ей следует перейти на приём тенофовира.
Наличие активного вирусного гепатита не является противопоказанием для кормления грудью независимо от того, находится кормящая грудью женщина на противовирусной терапии или нет, поскольку это не влияет на риск передачи гепатита B ребёнку [25] [26] .
Тенофовир, назначенный во втором или третьем триместре, может снизить риск передачи от матери к ребёнку на 77 % в сочетании с иммуноглобулином гепатита В и вакциной против гепатита В, особенно для беременных женщин с высоким уровнем ДНК вируса гепатита В [27] . Однако нет достаточных доказательств того, что введение одного лишь иммуноглобулина гепатита В во время беременности может снизить вероятность передачи вируса новорожденному [28] .
Бытовой путь [ править | править код ]
В семье или в организованном коллективе следует соблюдать обычные меры предосторожности [29] : не допускать пользование чужими средствами личной гигиены и с опаской относиться к чужой крови. Этим правилам нужно учить и детей. Опасность могут представлять кусачки и пилки для ногтей, зубные щётки, серьги, глюкометры и прочие. При уборке дома или автомобиля от загрязнения кровью необходимо пользоваться дезинфекционными средствами, а на руки надевать латексные перчатки или, в крайнем случае, полиэтиленовые пакеты. Любые повреждения кожи следует закрывать пластырем или повязкой.
Парентеральный путь [ править | править код ]
При инвазивных процедурах обязательно организовать [30] :
- использование перчаток;
- безопасное обращение и удаление острых предметов и отходов;
- безопасную очистку оборудования и инструментов;
- тестирование донорской крови;
- подготовку медицинского персонала;
- предотвращение повторного использования шприцев и прочих одноразовых предметов;
- принимать меры для уменьшения частоты травм от колющих и режущих инструментов у медицинских работников.
На государственном уровне ВОЗ рекомендует [30] работу с лицами, употребляющими внутривенные наркотики: программы выдачи игл и шприцев; опиоидную заместительную терапию; программы раздачи презервативов для людей, употребляющих инъекционные наркотики, и их сексуальных партнёров; вакцинацию, диагностику и лечение вирусного гепатита.
«>





