Hpv high risk
Содержание
- 1 HPV-инфекция у женщин – что это?
- 2 Пути передачи
- 3 Основные причины
- 4 Типы вируса
- 5 Проявления вируса
- 6 Характерная симптоматика
- 7 К чему приводит вирус?
- 8 Диагностика заболевания
- 9 Методы лечения
- 10 Терапия остроконечных кондилом
- 11 Противовирусная терапия папилломавирусной инфекции
- 12 Профилактика папилломавирусной инфекции
- 13 Содержание
- 14 Структура и белки [ править | править код ]
- 15 Классификация [ править | править код ]
- 16 Разновидности [ править | править код ]
- 17 Пути инфицирования [ править | править код ]
- 18 Формы существования папилломавирусов и течение болезни [ править | править код ]
- 19 Типы папилломавирусов по их клиническим проявлениям [ править | править код ]
- 20 Рак шейки матки [ править | править код ]
- 21 Диагностика [ править | править код ]
- 21.1 Клинический осмотр [ править | править код ]
- 21.2 Кольпоскопия [ править | править код ]
- 21.3 Цитологическое исследование шеечных мазков [ править | править код ]
- 21.4 Гистологическое исследование [ править | править код ]
- 21.5 Типирование с помощью ПЦР [ править | править код ]
- 21.6 Digene-тест [ править | править код ]
- 21.7 Исследование на заболевания, передающиеся половым путём [ править | править код ]
- 22 Лечение папилломавирусной инфекции [ править | править код ]
- 23 Профилактика генитальных инфекций [ править | править код ]
- 24 Key facts
- 25 What is HPV?
- 26 How HPV infection leads to cervical cancer
- 27 Risk factors for HPV persistence and development of cervical cancer
- 28 Global burden of cervical cancer
- 29 Cervical cancer control: A comprehensive approach
- 30 HPV vaccination
- 31 Screening and treatment of pre-cancer lesions
- 32 Management of invasive cervical cancer
- 33 WHO response
Все женщины мечтают выглядеть привлекательно. Но иногда кожа способна несколько огорчать представительниц прекрасного пола. Особенно неприятно, когда на ней появляются бородавки или малоэстетичные папилломы. Конечно, такой дефект барышни чаще всего воспринимают исключительно как внешний. А ведь эти образования вызывает неприятная, а иногда и опасная, HPV-инфекция у женщин. Что это такое? Как инфекция проникает в организм? Какими методами с ней бороться? Давайте разбираться.

HPV-инфекция у женщин – что это?
HPV на латыни обозначает название семейства вирусов: Human Papillomavirus. Сокращенная аббревиатура часто используется в медицине. Например, ее можно встретить в анализах.
Итак, если обнаружена HPV-инфекция у женщин, что это за патология? В переводе с латыни, это вирус папилломы человека (ВПЧ). Это большое семейство микроорганизмов. ВПЧ объединяет более 70 разновидностей вирусов. Они способны становиться источниками развития в организме различных заболеваний. Некоторые вирусы ВПЧ приводят к возникновению заболеваний кожи. Иные – провоцируют появление остроконечных кондилом. Сегодня медиками полностью установлена связь между наличием в организме женщины определенных видов ВПЧ и онкологией.
Данная инфекция достаточно опасна для организма. Она отличается слабовыраженной симптоматикой и при этом обладает внушительным инкубационным периодом. Поэтому ВПЧ может длительное время находиться в организме, ничем себя не выдавая. Особенно если речь идет о женщинах. Микрофлора влагалища – это благоприятная среда для вируса.
Основными особенностями HPV являются:
- латентность проявлений;
- долгий инкубационный период (иногда затягивающийся на несколько лет);
- слабовыраженная клиническая симптоматика;
- способность быстрой трансформации из папилломы в дисплазию.
Поскольку бородавки, кондиломы могут длительный период не доставлять женщине дискомфорта, патология на протяжении нескольких лет способна оставаться незамеченной. Но вы должны понимать, если выявлена HPV-инфекция у женщин, что это такое. Ведь в некоторых случаях, если своевременно не начато лечение ВПЧ, в организме развивается рак.
Согласно статистическим данным, около 70 % жителей земли инфицированы тем или иным видом ВПЧ.
Пути передачи
Существует всего 2 метода заражения ВПЧ:
- половой (наиболее распространенный);
- бытовой.
Инфекция HPV у женщин может быть спровоцирована следующими причинами:
- Половой контакт с инфицируемой особой. И даже презерватив не всегда становится достаточным средством защиты. Во время оральных ласк высок риск заражения ВПЧ.
- Процедуры в косметологическом салоне. К сожалению, на втором месте стоит именно этот путь заражения вирусом. Инфицирование происходит через недостаточно обеззараженный инструментарий. Чаще всего ВПЧ проникает в организм после процедуры перманентного макияжа либо эпиляции участка бикини. Чтобы защитить себя от риска инфекции, можно попросить продезинфицировать инструменты при вас либо требовать использования исключительно одноразовых предметов.
- Несоблюдение личной гигиены. Если средства для индивидуального туалета используются другими членами семьи, то высок риск заражения. Каждый человек должен обладать своими вещами личной гигиены. Это касается всех предметов: мочалки, полотенца, пемзы, пинцета, маникюрных ножничек.
Основные причины
Таким образом, инфекция HPV у женщин чаще всего проникает именно половым путем. Однако нельзя исключать риск заражения через дружеские поцелуи, рукопожатия и даже бытовые предметы. Через небольшие повреждения кожи либо слизистой возбудитель легко проникает в организм.
А выявить на ранних сроках патологию практически невозможно. Ведь вирус может длительное время быть в наличии, но в скрытой форме. В некоторых случаях инкубационный период достигает даже до трех месяцев.
Существует несколько факторов, на фоне которых чаще всего развивается HPV-инфекция у женщин. Причины инфицирования медики приводят следующие:
- частая смена сексуальных партнеров;
- постоянный стресс;
- курение;
- авитаминоз, значительное снижение иммунитета;
- алкоголизм;
- раннее начало половой регулярной жизни;
- нарушенное протекание обменных процессов;
- болезни ЖКТ (гастрит);
- гинекологические недуги (уреаплазмоз, молочница, эрозия шейки матки, гонорея, трихомоноз, хламидиоз);
- частое посещение мест, с высоким риском заражения (бани, сауны, бассейны);
- изменения в гормональном фоне в результате употребления противозачаточных препаратов.
Типы вируса
В семейство ВПЧ входит множество разновидностей вирусов. Именно от вида микроорганизма зависит, как будет проявляться HPV-инфекция у женщин.
Типы вируса классифицируют следующим образом:
- ВПЧ, лежащие в основе появления бородавок. Типы от 1-го до 4-го приводят к образованию подошвенных бородавок. Они напоминают мозоль. Благодаря 3, 10, 28 и 49-му типу появляются плоские бородавки. А к возникновению обыкновенных образований приводит 27-й тип.
- ВПЧ, затрагивающие дыхательные пути, половые органы. В поражении данных органов виновны 6, 11, 13, 16, 18, 31, 33, 35-й типы.
- ВПЧ, которые провоцируют предраковое состояние. Это типы, обладающие высоким онкогенным риском. К данной категории относят 30, 39, 40, 42, 43, 55, 57, 61, 62, 64, 67, 69, 70-й.
Проявления вируса
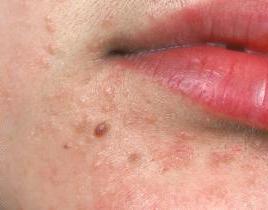
Конечно, определить тип можно только при помощи лабораторных методов исследования. Но при этом даже по внешнему виду можно заподозрить, что имеет место HPV-инфекция у женщин. Фото, приведенное в статье, показывает, с какими внешними проявлениями может столкнуться инфицированная особа.
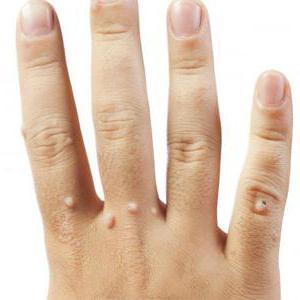
Итак, папилломавирусная инфекция может проявляться следующим образом:
- Остроконечные кондиломы. Такие образования чаще всего провоцируют вирусы с низким онкогенным риском. Генитальные кондиломы могут быть очаговыми либо единичными. Они появляются на тех участках, которые во время полового акта травмируются. Размер этих образований – от 1 мм до нескольких сантиметров. Они располагаются на узкой «ножке». По своему виду могут напоминать «цветную капусту» либо «петушиный гребень». Чаще всего они обнаруживаются случайно, во время личной гигиены, как неровность слизистой. Иногда женщины могут травмировать кондилому. В этом случае она кровоточит, вызывает дискомфорт при половом акте либо родах.
- Папилломы. Это бородавочные образования. Вирусные папилломы, в отличие от опухолевых, могут возникать, затем исчезать. Появление этих образований зависит от силы иммунитета в настоящее время. Вирусные папилломы способны вырасти на любом участке. По цвету они практически не отличаются от нормального оттенка кожи.
- Плоские кондиломы шейки матки. Они сигнализируют о наличии застарелой инфекции в организме. В этом случае может наблюдаться изменение эпителия шейки матки на клеточном уровне. Такие нарушения вызывают серьезные опасения у доктора. Ведь именно эти изменения нередко приводят к развитию онкологии. Однако наличие в организме вируса – это не 100 % вероятность развития рака. Онкология появляется только в том случае, если присутствуют дополнительные факторы, способствующие перерождению доброкачественных клеток в злокачественные.
Характерная симптоматика
Какими признаками может сигнализировать о себе HPV-инфекция у женщин?
Симптомы, на которые обязательно следует обратить внимание:
- появление зуда, неприятного жжения в районе половых органов;
- наличие постоянных выделений (белых, желто-зеленых, сукровичных);
- небольшое увеличение лимфоузлов;
- множественные образования (папилломы, бородавки) на разных участках тела.
При наличии даже нескольких симптомов обязательно обратитесь к гинекологу для обследования.

К чему приводит вирус?
Данная инфекция крайне опасна теми последствиями, которые она способна спровоцировать без адекватного лечения.
В некоторых случаях могут развиться следующие осложнения:
- рак головы;
- гиперплазия слизистой ротовой полости;
- рак шеи;
- папилломатоз дыхательных путей;
- онкология лёгких.
Если речь идет о половых органах, то вирус способен привести к развитию:
- онкологии шейки матки;
- дисплазии;
- раку ануса;
- онкологии влагалища или наружных органов.
Диагностика заболевания
Теперь рассмотрим, как определяется HPV-инфекция у женщин.
Диагностика подразумевает комплексный подход и включает такие мероприятия:
- Осмотр у гинеколога. Женщины должны регулярно посещать врача. Даже обычный осмотр способен помочь выявить ВПЧ.
- Кольпоскопия. Такое исследование проводится при помощи специального микроскопа. Кольпоскоп во много раз увеличивает женские органы. Это позволяет отлично рассмотреть кондиломы. Применение дополнительных веществ помогает констатировать ВПЧ.
- Цитологический мазок. Соскоб позволяет детально изучить ткани под микроскопом. Исследование дает возможность определить начальные стадии рака. Обязательно назначается данное обследование при дисплазии. Оно называется тестом Папаниколау.
- Биопсия. Маленький фрагмент ткани матки изучается под большим увеличением. Проведение биопсии категорически противопоказано беременным.
- Гистологическое исследование. Позволяет изучить строение клеток и расположение слоев. Образец ткани изначально проходит специальную подготовку и только затем тщательно анализируется.
- ПЦР. Анализ дает представление о типе вируса и позволяет определить его онкогенность.
Методы лечения
Единой программы для лечения ВПЧ не существует. Для каждого конкретного случая подбирается своя терапия. При этом даже комплексное лечение не способно полностью избавить пациента от данного недуга.
Терапия остроконечных кондилом
Основной способ борьбы – механическое удаление. Какие же методы наиболее эффективны, если диагностируется HPV-инфекция у женщин? Описание процедуры, приведенное к каждому способу, позволит понять суть данного вмешательства.
Итак, для терапии остроконечных кондилом предпринимаются:
- Лазеротерапия. Дефекты удаляют под местной анестезией. Процедура производится лазером.
- Криодеструкция. Неприятные дефекты удаляются при помощи жидкого азота. Процедура совершенно безболезненна и не оставляет после себя рубцов.
- Электрокоагуляция. Терапия производится при помощи электрического тока. Метод достаточно болезненный.
- Радиоволновая коагуляция. Процедура обладает отличным лечебным результатом, проводится под местным обезболиванием. Кондиломы удаляют при помощи радиоволнового ножа.
- Хирургическое удаление. Крайне редкий метод лечения. Используется только при озлокачествлении тканей.
Противовирусная терапия папилломавирусной инфекции
Специального лечения не разработано. Поэтому пациенту назначают противовирусные средства, стимулирующие иммунитет:
- Лекарства, блокирующие размножение вируса и активизирующие иммунную систему. Эффективными препаратами являются «Изопринозин», «Инозиплекс».
- Интерфероны. Медикаменты обеспечивают противовирусное воздействие, способствуют повышению иммунитета. Кроме того, им присущ противоопухолевый эффект. Такими лекарствами являются «Интрон-А», «Альфа-интерферон», «Генферон».
- Препараты, активизирующие в организме вырабатывание собственных интерферонов. Могут быть порекомендованы лекарства «Циклоферон», «Амиксин».
- Медикаменты, предупреждающие размножение клеток, пораженных вирусом. Отличными препаратами являются «Подофиллин», «Кондилин», «Подофиллотоксин».
Однако ни один из перечисленных выше препаратов не способен полностью излечить от инфекции.
Профилактика папилломавирусной инфекции
Эта тема сегодня крайне актуальна. Не забывайте, что к раку шейки матки может привести именно HPV-инфекция у женщин.
Методы профилактики включают:
- неспецифические способы;
- специфические.
В первом случае речь идет о половом воспитании подрастающего поколения. Очень важно объяснить, как защитить организм и какими способами передается HPV-инфекция у женщин.
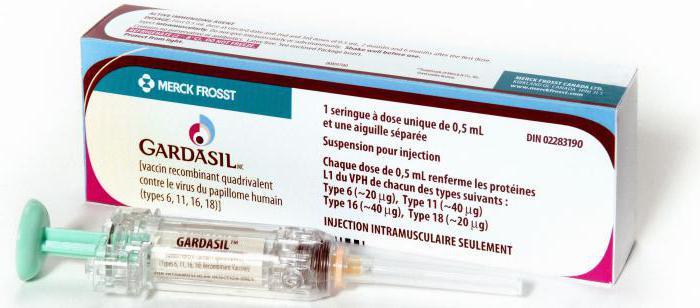
Профилактика специфическая – это вакцинирование, направленное на защиту от самых онкогенных типов вируса. Сформированный после прививки стойкий иммунитет позволяет защитить женщину от рака. Подобная вакцинация рекомендована девушкам до начала половой жизни.
Самими эффективными и признанными во всем мире вакцинами против ВПЧ являются:
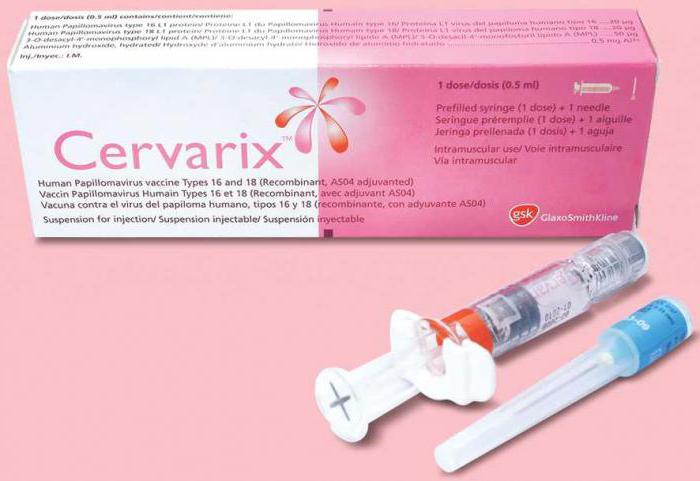
Данные прививки делают и в том случае, если женщина уже ведет половую жизнь. Однако перед вакцинацией ей необходимо пройти назначенное доктором обследование для исключения вероятности наличия в организме ВПЧ.

| Полифилетическая группа вирусов | |
|---|---|
 |
|
| Название | |
| Папилломавирусы человека | |
| Статус названия | |
| Устаревшее таксономическое | |
| Научное название | |
| Human papillomavirus | |
| Родительский таксон | |
| Семейство Papillomaviridae | |
| Виды | |
| Изображения на Викискладе |
| Папилломавирус человека | |
|---|---|
 |
|
| МКБ-10 | B 97.7 97.7 |
| МКБ-9 | 078.1 078.1 079.4 079.4 |
| МКБ-9-КМ | 079.4 [1] |
| DiseasesDB | 6032 |
| eMedicine | med/1037 |
| MeSH | D030361 |
Содержание
Структура и белки [ править | править код ]
Папилломавирусы имеют видоспецифические и некоторые типоспецифические антигены. Не культивируются в клеточных системах. Вирус папилломы человека выявляется в кератоцитах в виде эписомы, 50—200 копий на поражённую клетку. Процессы продуктивной инфекции и интеграции не наблюдаются.
Классификация [ править | править код ]
Группа была зарегистрирована Международным комитетом по таксономии вирусов (ICTV) как единый вид Human papilloma virus в 1971 году [5] . В 2003 его окончательно разделили на 27 видов в 5 родах [3] , а в 2010 эти виды переименовали так, чтобы их научные названия отражали род, к которому они относятся [6] . Все виды папилломавирусов человека, зарегистрированные в 2003 году, сведены в таблицу ниже.
| Название вида в 2003—2010 гг. [3] | Другие типы (штаммы), включённые в вид [3] | Название вида с 2010 г. [6] |
|---|---|---|
| Human papillomavirus 1 (HPV1) | — | Mupapillomavirus 1 |
| Human papillomavirus 2 (HPV2) | HPV27, HPV57 | Alphapapillomavirus 4 |
| Human papillomavirus 4 (HPV4) | HPV65, HPV95 | Gammapapillomavirus 1 |
| Human papillomavirus 5 (HPV5) | HPV8, HPV12, HPV14, HPV19, HPV20, HPV21, HPV25, HPV36, HPV47 | Betapapillomavirus 1 |
| Human papillomavirus 6 (HPV6) | HPV11, HPV13, HPV44, HPV74, PcPV | Alphapapillomavirus 10 |
| Human papillomavirus 7 (HPV7) | HPV40, HPV43, HPV91 | Alphapapillomavirus 8 |
| Human papillomavirus 9 (HPV9) | HPV15, HPV17, HPV22, HPV23, HPV37, HPV38, HPV80 | Betapapillomavirus 2 |
| Human papillomavirus 10 (HPV10) | HPV3, HPV28, HPV29, HPV77, HPV78, HPV94 | Alphapapillomavirus 2 |
| Human papillomavirus 16 (HPV16) | HPV31, HPV33, HPV35, HPV52, HPV58, HPV67 | Alphapapillomavirus 9 |
| Human papillomavirus 18 (HPV18) | HPV39, HPV45, HPV59, HPV68, HPV70, HPV85 | Alphapapillomavirus 7 |
| Human papillomavirus 26 (HPV26) | HPV51, HPV69, HPV82 | Alphapapillomavirus 5 |
| Human papillomavirus 32 (HPV32) | HPV42 | Alphapapillomavirus 1 |
| Human papillomavirus 34 (HPV34) | HPV73 | Alphapapillomavirus 11 |
| Human papillomavirus 41 (HPV41) | — | Nupapillomavirus 1 |
| Human papillomavirus 48 (HPV48) | — | Gammapapillomavirus 2 |
| Human papillomavirus 49 (HPV49) | HPV75, HPV76 | Betapapillomavirus 3 |
| Human papillomavirus 50 (HPV50) | — | Gammapapillomavirus 3 |
| Human papillomavirus 53 (HPV53) | HPV30, HPV56, HPV66 | Alphapapillomavirus 6 |
| Human papillomavirus 54 (HPV54) | — | Alphapapillomavirus 13 |
| Human papillomavirus 60 (HPV60) | — | Gammapapillomavirus 4 |
| Human papillomavirus 61 (HPV61) | HPV72, HPV81, HPV83, HPV84, HPVcand62, HPVcand86, HPVcand87, HPVcand89 | Alphapapillomavirus 3 |
| Human papillomavirus 63 (HPV63) | — | Mupapillomavirus 2 |
| Human papillomavirus 71 (HPV71) | — | удалён |
| Human papillomavirus 88 (HPV88) | — | Gammapapillomavirus 5 |
| Human papillomavirus cand90 (HPVcand90) | — | Alphapapillomavirus 14 |
| Human papillomavirus cand92 (HPVcand92) | — | Betapapillomavirus 4 |
Разновидности [ править | править код ]
Папилломавирусы человека известны достаточно давно, именно они вызывают бородавки.
В настоящее время известно уже более 600 типов (штаммов) папилломавирусов, обнаруженных у человека. Из них более 40 могут вызвать поражение аногенитального тракта (половые органы и перианальная область) мужчин и женщин и появление остроконечных кондилом. Одни из них безвредны, другие вызывают бородавки, некоторые вызывают рак.
Некоторые представители группы обладают онкогенными свойствами и в редких случаях вызывают трансформации тканей, доброкачественные или злокачественные опухоли. В 1980-х годах стали появляться сообщения об том, что папилломавирусы вызывают рак шейки матки, которые впоследствии были доказаны убедительной статистикой [7] .
В 2006 году в российских СМИ появилось сообщение, что австралийскими учёными установлена взаимосвязь рака молочной железы с вирусом папилломы человека [8] [ неавторитетный источник? ] . Но исследователи не обнаружили ВПЧ в опухолях молочных желёз [9]
К 2017 году выявлена и доказана роль ВПЧ в онкологических заболеваниях: рак шейки матки, рак ануса у женщин и мужчин, рак влагалища и рак пениса (в порядке убывания частоты), в 2010 году доказана взаимосвязь между папилломавирусной инфекцией и развитием плоскоклеточного рака рта и глотки. Есть противоречивые данные о роли ВПЧ в развитии рака мочевого пузыря. [10]
Ряд исследователей заявляют о возможности мутации вируса из одного типа в другой внутри организма человека. Но пока ВОЗ не закрепила эти исследования в виде рекомендаций.
Пути инфицирования [ править | править код ]
- Основным путём заражения аногенитальными бородавками (остроконечными кондиломами) является половой путь заражения.
- Возможно заражение папилломавирусом новорождённых при родах, что является причиной возникновения ларингеального папилломатоза у детей и аногенитальных бородавок у младенцев.
- Возможно заражение бытовым путём, например, через прикосновение. Вирус папилломы человека способен существовать некоторое время в общественных местах (туалеты, бани, бассейны, спортзалы) и проникать в организм человека через ссадины и царапины на коже [11][12] .
- Возможно самозаражение (аутоинокуляция) при бритье, эпиляции [12] .
Формы существования папилломавирусов и течение болезни [ править | править код ]

Попав в организм, вирусы папиллом инфицируют базальный слой эпителия, причём наиболее поражённым участком является зона перехода многослойного плоского эпителия в цилиндрический эпителий.
В заражённой клетке вирус существует в двух формах: эписомальной (вне хромосом клетки), которая считается доброкачественной формой, и интросомальной — интегрированной (встраиваясь в геном клетки) — которую определяют как злокачественную форму паразитирования вируса.
Течение болезни [ править | править код ]
Инкубационный период — длительный: от половины месяца [ источник не указан 89 дней ] до нескольких лет [ источник не указан 89 дней ] . Для папилломавирусной инфекции характерно скрытое (латентное) течение. [ источник не указан 89 дней ] Человек может одновременно заражаться несколькими типами папилломавирусов. [ источник не указан 89 дней ] Под влиянием различных [ каких? ] факторов происходит активация вируса, его усиленное размножение, и болезнь переходит в стадию клинических проявлений. [ источник не указан 89 дней ]
В большинстве случаев (до 90 % [ источник не указан 89 дней ] ) в течение 6 [ источник не указан 89 дней ] —12 [ источник не указан 89 дней ] месяцев [ источник не указан 89 дней ] происходит самоизлечение [ источник не указан 89 дней ] , в других случаях отмечается длительное хроническое [ источник не указан 89 дней ] рецидивирующее [ источник не указан 89 дней ] течение с возможной малигнизацией процесса (в зависимости от типа вируса). [ источник не указан 89 дней ]
Специфической терапии инфекции ВПЧ не существует, в большинстве случаев инфицирование не вызывает проблем и организм излечивается сам в течение двух лет [13] , но может проявиться повторно, в частности, можно заразиться другим штаммом вируса [14] .
Типы папилломавирусов по их клиническим проявлениям [ править | править код ]
На основании способности индуцировать неопластические процессы папилломавирусы классифицируют на три группы [15] :
- Онкогенные папилломавирусы низкого онкогенного риска (HPV 3, 6, 11, 13, 32, 34, 40, 41, 42, 43, 44, 51, 61, 72, 73)
- Онкогенные папилломавирусы среднего онкогенного риска (HPV 30, 35, 45, 52, 53, 56, 58)
- Онкогенные папилломавирусы высокого онкогенного риска (HPV 16, 18, 31, 33, 39, 50, 59, 64, 68, 70).
Из них при раке шейки матки в 95 % находят ВПЧ около 20 типов, наиболее часто 16 и 18 типов — 50 и 10 % соответственно [15] .
Рак шейки матки [ править | править код ]
Рак шейки матки (плоскоклеточная карцинома, Cervical cancer). При отсутствии вируса заболевание раком шейки матки не встречается. Развитие заболевания медленное, поэтому оно выявляется через десятилетия (Greenblatt, 2005; Sinal and Woods, 2005)Шаблон:ВОЗ о ВПЧ.
Высокий риск HPV-16 и 18, встречается в 70 % случаев (Baseman and Koutsky, 2005; Cohen, 2005). Тип 16 даёт 41—54 % случаев рака (Noel et al., 2001; Baseman and Koutsky, 2005).
Диагностика [ править | править код ]
Клинический осмотр [ править | править код ]
По характерной клинической картине выявляются все виды бородавок, остроконечные кондиломы. При наличии аногенитальных бородавок обязателен осмотр шейки матки, по показаниям — для исключения эндоуретральных кондилом — уретроскопия.
Кольпоскопия [ править | править код ]
Кольпоскопия и биопсия показаны всем женщинам с цервикальной интраэпителиальной неоплазией класса II(CIN II) или класса III(CIN III), независимо от подтверждения у них наличия ВПЧ-инфекции.
Проводится тест с уксусной кислотой (Acetic Acid Test). В настоящее время специфическим кольпоскопическим признаком ПВИ шейки матки считается неравномерное поглощение йодного раствора Люголя беловатым после уксуса участком эпителия (в виде йодпозитивных пунктации и мозаики). Признаками ПВИ шейки матки могут также быть ацетобелый эпителий, лейкоплакия, пунктация, белые выросты и мозаика, атипичная зона трансформации, жемчужная поверхность после обработки уксусом.
Цитологическое исследование шеечных мазков [ править | править код ]
Цитологическое исследование шеечных мазков по Папаниколау (PAP — smear test) выделяет следующие результаты:
- 1-й класс — атипические клетки отсутствуют, нормальная цитологическая картина;
- 2-й класс — изменение клеточных элементов обусловлено воспалительным процессом во влагалище и (или) шейке матки;
- 3-й класс — имеются единичные клетки с изменениями соотношения ядра и цитоплазмы, диагноз недостаточно ясен, требуется повторение цитологического исследования или необходимо гистологическое исследование биоптированной ткани для изучения состояния шейки матки;
- 4-й класс — обнаруживаются отдельные клетки с признаками злокачественности, а именно с увеличенными ядрами и базофильной цитоплазмой, неравномерным распределением хроматина;
- 5-й класс — в мазке имеются многочисленные атипические клетки.
Гистологическое исследование [ править | править код ]

Обнаруживается умеренное утолщение рогового слоя с папилломатозом (не путать с микропапилломатозом), паракератозом и акантозом; могут присутствовать фигуры митоза. Диагностически важным считается наличие в глубоких участках мальпигиева слоя койлоцитов — больших эпителиальных клеток с круглыми гиперхромными ядрами и выраженной перинуклеарной вакуолизацией.
Типирование с помощью ПЦР [ править | править код ]
Метод ПЦР имеет большую диагностическую значимость и позволяет идентифицировать отдельные типы ВПЧ. Однако использование этого метода как диагностического критерия для неопластических процессов шейки матки приводит к значительной гипердиагностике, так как примерно в 80 % случаев инфицирование имеет кратковременный характер и заканчивается спонтанным выздоровлением и элиминацией вируса. Так, по данным западных независимых лабораторий, результаты ПЦР к ВПЧ давали ложноположительные или ложноотрицательные результаты почти в 20 % случаев. Таким образом, положительный результат при лабораторном исследовании на ДНК ВПЧ не позволяет в большинстве случаев прогнозировать развитие цервикального рака. Однако он имеет большую прогностическую значимость, особенно если на фоне ВПЧ-инфекции уже имеется картина дисплазии эпителия шейки матки, и позволяет говорить о степени канцерогенного риска.
Digene-тест [ править | править код ]
Скрининговый тест, принятый во всех странах мира. Используется для быстрого выявления клинически значимых концентраций высоконкогенных типов папилломавируса. Имеет высокую специфичность и точность диагностики. Оценка теста производится в комплексе с цитологическим исследованием шейки матки.
Исследование на заболевания, передающиеся половым путём [ править | править код ]
Так как аногенитальные бородавки в 90 % случаев ассоциируются с другими урогенитальными инфекциями, целесообразно проводить исследования на их наличие методом ПЦР.
Лечение папилломавирусной инфекции [ править | править код ]
Радикальной терапии папилломавируса не существует [16] [17] [18] , то есть нет препаратов и методов, которые бы позволяли устранить вирус из организма человека полностью. Врачи лечат только последствия действия вируса, то есть удаляют бородавки, первичные стадии раковых заболеваний (ткани с клеточными изменениями). Общая терапия назначается при поражении высокоонкогенными типами вируса с локализацией патологического процесса в области аногенитального тракта. В качестве препаратов выбора используются противовирусные препараты и иммуномодуляторы.
Согласно исследованиям Центров по контролю и профилактике заболеваний США, естественный иммунитет самостоятельно справляется с вирусом в организме в течение 2 лет в 90 % случаев [16] .
Средствами удаления поражённых тканей могут быть:
Побочным эффектом может быть распространение вируса на прилегающие ткани, повреждённые в процессе удаления поражённых участков.
Перспективным направлением в лечении вирусных заболеваний, включая ВПЧ, является генная терапия, варианты CRISPR/Cas9 и "цинковые пальцы".
Профилактика генитальных инфекций [ править | править код ]
Несмотря на появляющиеся результаты исследований о неполной эффективности применения — барьерная контрацепция (презерватив) остаётся легкодоступным средством возможного, но не полного предохранения от папилломавирусной инфекции человека (поскольку презерватив может изолировать не все соприкасающиеся участки повреждённой кожи).
В США разработана вакцина Gardasil, которая рекомендована 16 июня 2006 года Консультативный комитет по практике иммунизации (англ. Advisory Committee on Immunization Practices, ACIP ) [19] к применению как защита от рака шейки матки и других заболеваний женщин, вызываемых ВПЧ [20] . Вакцина эффективна против четырёх видов вируса ВПЧ: 6, 11, 16 и 18 [21] . Вакцинация проводится девочкам, начиная с 11—12 лет, троекратно. Цена 1 инъекции — 120 долларов США (360 для полной иммунизации). Подобная вакцина применяется и в некоторых странах Европы, (например Греции, но уже по цене 185 евро за инъекцию в 2007 г. [22] ). Вакцинация против ВПЧ проводится в Израиле как часть рутинной программы вакцинации на станциях «Типат Халав» и в школах бесплатно, причём не только девочкам, но и мальчикам [23] [24] . В России вакцина Гардасил зарегистрирована в 2006 году и также доступна для применения.
Другая вакцина — Церварикс, эффективна для ВПЧ 16 и 18 [25] — появилась на рынке позже, доступна и разрешена для применения с 10 лет.
С 2016 года прививка от ВПЧ входит в календари (обязательных, оплаченных из бюджета, и рекомендованных, вакцина оплачивается пациентом) прививок многих регионов России: Москвы [26] (по региональному календарю в 12—13 лет, бесплатно для пациентов в любом возрасте) [27] , Свердловской области [28] (при этом вакцина не входит в перечень закупаемых областным бюджетом) [29] , Челябинской области [30] и др. В регионах, где прививка не входит в календарь, за неё надо платить, например, в Рязани 4700—10000 руб. в 2019 г. [31] В большинстве регионов используется вакцина Гардасил [ источник не указан 129 дней ] .
Российские специалисты говорят о необходимости проведения вакцинации против ВПЧ на национальном уровне [32] .
ВОЗ рекомендует вакцинировать не только девочек, но и мальчиков с целью предотвратить циркулирование вируса [33] . В Австралии с 2007 г. прививают девочек и с 2011 г. — мальчиков, в результате в 2018 году на 92% снизилось инфицирование населения наиболее онкогенными видами ВПЧ [32] .
В 2018 г. CDC США разрешило вакцинацию для мужчин и женщин старше 27 лет, вплоть до 45 лет. Раньше ее считали эффективной только до 27 лет [14] [34] . По данным на конец 2018 года вакцинация женщин эффективна вплоть до достижения ими 50 лет [32] .
Key facts
- Human papillomavirus (HPV) is a group of viruses that are extremely common worldwide.
- There are more than 100 types of HPV, of which at least 14 are cancer-causing (also known as high risk type).
- HPV is mainly transmitted through sexual contact and most people are infected with HPV shortly after the onset of sexual activity.
- Cervical cancer is caused by sexually acquired infection with certain types of HPV.
- Two HPV types (16 and 18) cause 70% of cervical cancers and pre-cancerous cervical lesions.
- There is also evidence linking HPV with cancers of the anus, vulva, vagina, penis and oropharynx.
- Cervical cancer is the second most common cancer in women living in less developed regions with an estimated 570 000 new cases (1) in 2018 (84% of the new cases worldwide).
- In 2018, approximately 311 000 women died from cervical cancer; more than 85% of these deaths occurring in low- and middle-income countries.
- Comprehensive cervical cancer control includes primary prevention (vaccination against HPV), secondary prevention (screening and treatment of pre-cancerous lesions), tertiary prevention (diagnosis and treatment of invasive cervical cancer) and palliative care.
- Vaccines that protect against HPV 16 and 18 are recommended by WHO and have been approved for use in many countries.
- Screening and treatment of pre-cancer lesions in women of 30 years and more is a cost-effective way to prevent cervical cancer.
- Clinical trials and post-marketing surveillance have shown that HPV vaccines are very safe and very effective in preventing infections with HPV infections.
- Cervical cancer can be cured if diagnosed at an early stage.
What is HPV?
Human papillomavirus (HPV) is the most common viral infection of the reproductive tract. Most sexually active women and men will be infected at some point in their lives and some may be repeatedly infected.
The peak time for acquiring infection for both women and men is shortly after becoming sexually active. HPV is sexually transmitted, but penetrative sex is not required for transmission. Skin-to-skin genital contact is a well-recognized mode of transmission.
There are many types of HPV, and many do not cause problems. HPV infections usually clear up without any intervention within a few months after acquisition, and about 90% clear within 2 years. A small proportion of infections with certain types of HPV can persist and progress to cervical cancer.
Cervical cancer is by far the most common HPV-related disease. Nearly all cases of cervical cancer can be attributable to HPV infection.
The infection with certain HPV types also causes a proportion of cancers of the anus, vulva, vagina, penis and oropharynx, which are preventable using similar primary prevention strategies as those for cervical cancer.
Non-cancer causing types of HPV (especially types 6 and 11) can cause genital warts and respiratory papillomatosis (a disease in which tumours grow in the air passages leading from the nose and mouth into the lungs). Although these conditions very rarely result in death, they may cause significant occurrence of disease. Genital warts are very common, highly infectious and affect sexual life.
How HPV infection leads to cervical cancer
Although most HPV infections clear up on their own and most pre-cancerous lesions resolve spontaneously, there is a risk for all women that HPV infection may become chronic and pre-cancerous lesions progress to invasive cervical cancer.
It takes 15 to 20 years for cervical cancer to develop in women with normal immune systems. It can take only 5 to 10 years in women with weakened immune systems, such as those with untreated HIV infection.
Risk factors for HPV persistence and development of cervical cancer
- HPV type – its oncogenicity or cancer-causing strength;
- immune status – people who are immunocompromised, such as those living with HIV, are more likely to have persistent HPV infections and a more rapid progression to pre-cancer and cancer;
- coinfection with other sexually transmitted agents, such as those that cause herpes simplex, chlamydia and gonorrhoea;
- parity (number of babies born) and young age at first birth;
- tobacco smoking
Global burden of cervical cancer
Worldwide, cervical cancer is the fourth most frequent cancer in women with an estimated 570 000 new cases in 2018 representing 7.5% of all female cancer deaths. Of the estimated more than 311 000 deaths from cervical cancer every year, more than 85% of these occur in less developed regions.
In developed countries, programmes are in place which enable girls to be vaccinated against HPV and women to get screened regularly. Screening allows pre-cancerous lesions to be identified at stages when they can easily be treated. Early treatment prevents up to 80% of cervical cancers in these countries.
In developing countries, there is limited access to these preventative measures and cervical cancer is often not identified until it has further advanced and symptoms develop. In addition, access to treatment of such late-stage disease (for example, cancer surgery, radiotherapy and chemotherapy) may be very limited, resulting in a higher rate of death from cervical cancer in these countries.
The high mortality rate from cervical cancer globally (Age Standardized Rate: 6.9/100,000 in 2018) could be reduced by effective interventions.
Cervical cancer control: A comprehensive approach
WHO recommends a comprehensive approach to cervical cancer prevention and control. The recommended set of actions includes interventions across the life course. It should be multidisciplinary, including components from community education, social mobilization, vaccination, screening, treatment and palliative care. 
Primary prevention
Secondary prevention
Tertiary prevention
- HPV vaccination
- Health information and warnings about tobacco use
- Sex education tailored to age and culture
- Condom promotion and provision for those engaged in sexual activity
- Male circumcision
- Point-of-care rapid HPV testing for high-risk HPV types
- Followed by immediate treatment
- On-site treatment
- Surgery
- Radiotherapy
- Chemotherapy
- Palliative care
Primary prevention begins with HPV vaccination of girls aged 9-14 years, before they become sexually active.
Other recommended preventive interventions for boys and girls as appropriate are:
- education about safe sexual practices, including delayed start of sexual activity;
- promotion and provision of condoms for those already engaged in sexual activity;
- warnings about tobacco use, which often starts during adolescence, and which is an important risk factor for cervical and other cancers; and
- male circumcision.
Women who are sexually active should be screened for abnormal cervical cells and pre-cancerous lesions, starting from 30 years of age.
If treatment of pre-cancer is needed to excise abnormal cells or lesions, cryotherapy (destroying abnormal tissue on the cervix by freezing it) is recommended.
If signs of cervical cancer are present, treatment options for invasive cancer include surgery, radiotherapy and chemotherapy.
HPV vaccination
There are currently 3 vaccines protecting against both HPV 16 and 18, which are known to cause at least 70% of cervical cancers. The third vaccine protects against three additional oncogentic HPV types, which cause a further 20% of cervical cancers. Given that the vaccines which are only protecting against HPV 16 and 18 also have some cross-protection against other less common HPV types which cause cervical cancer, WHO considers the three vaccines equally protective against cervical cancer. Two of the vaccines also protect against HPV types 6 and 11, which cause anogenital warts.
Clinical trials and post-marketing surveillance have shown that HPV vaccines are very safe and very effective in preventing infections with HPV infections.
HPV vaccines work best if administered prior to exposure to HPV. Therefore, WHO recommends to vaccinate girls, aged between 9 and 14 years, when most have not started sexual activity.
The vaccines cannot treat HPV infection or HPV-associated disease, such as cancer.
Some countries have started to vaccinate boys as the vaccination prevents genital cancers in males as well as females, and two available vaccines also prevent genital warts in males and females. WHO recommends vaccination for girls aged between 9 and 14 years, as this is the most cost-effective public health measure against cervical cancer.
HPV vaccination does not replace cervical cancer screening. In countries where HPV vaccine is introduced, screening programmes may still need to be developed or strengthened.
Screening and treatment of pre-cancer lesions
Cervical cancer screening involves testing for pre-cancer and cancer among women who have no symptoms and may feel perfectly healthy. When screening detects pre-cancerous lesions, these can easily be treated, and cancer can be avoided. Screening can also detect cancer at an early stage and treatment has a high potential for cure.
Because pre-cancerous lesions take many years to develop, screening is recommended for every woman from aged 30 and regularly afterwards (frequency depends on the screening test used). For women living with HIV who are sexually active, screening should be done earlier, as soon as they know their HIV status.
Screening has to be linked to access to treatment and management of positive screening tests. Screening without proper management is not ethical.
There are 3 different types of screening tests that are currently recommended by WHO:
- HPV testing for high-risk HPV types.
- visual inspection with Acetic Acid (VIA)
- conventional (Pap) test and liquid-based cytology (LBC)
For treatment of pre-cancer lesions, WHO recommends the use of cryotherapy and Loop Electrosurgical Excision Procedure (LEEP). For advanced lesions, women should be referred for further investigations and adequate management.
Management of invasive cervical cancer
When a woman presents symptoms of suspicion for cervical cancer, she must be referred to an appropriate facility for further evaluation, diagnosis and treatment.
Symptoms of early stage cervical cancer may include:
- Irregular blood spotting or light bleeding between periods in women of reproductive age;
- Postmenopausal spotting or bleeding;
- Bleeding after sexual intercourse; and
- Increased vaginal discharge, sometimes foul smelling.
As cervical cancer advances, more severe symptoms may appear including:
- Persistent back, leg and/or pelvic pain;
- Weight loss, fatigue, loss of appetite;
- Foul-smell discharge and vaginal discomfort; and
- Swelling of a leg or both lower extremities.
Other severe symptoms may arise at advanced stages depending on which organs cancer has spread.
Diagnosis of cervical cancer must be made by histopathologic examination. Staging is done based on tumor size and spread of the disease within the pelvis and to distant organs. Treatment depends on the stage of the disease and options include surgery, radiotherapy and chemotherapy. Palliative care is also an essential element of cancer management to relive unnecessary pain and suffering due the disease.
WHO response
WHO has developed guidance on how to prevent and control cervical cancer through vaccination, screening and management of invasive cancer. WHO works with countries and partners to develop and implement comprehensive programmes.
In May 2018 the WHO Director-General made a call to action towards the elimination of cervical cancer and engage partners and countries to increase access to and coverage of these 3 essential interventions to prevent cervical cancer: HPV vaccination, screening and treatment of pre-cancer lesions, and management of cervical cancer.


