Ожирение и беременность научные статьи
*Импакт фактор за 2017 г. по данным РИНЦ
Журнал входит в Перечень рецензируемых научных изданий ВАК.

Читайте в новом номере
В статье рассмотрены вопросы влияния ожирения у женщин на фертильность и вынашивание беременности

Для цитирования. Иловайская И.А. Влияние ожирения у женщин на фертильность и вынашивание беременности // РМЖ. 2016. No 1. С. 32–37.
Беременность у женщины с ожирением ассоциирована с рядом материнских и перинатальных рисков. Степень и частота этих рисков увеличиваются в зависимости от выраженности ожирения. Снижение массы тела у женщин репродуктивного возраста, планирующих беременность, и потенциальное уменьшение этих рисков являются важными задачами интернистов и акушеров-гинекологов.
Ожирение характеризуется избыточным содержанием в организме жировой ткани. Индекс массы тела (ИМТ) прямо коррелирует с массой жировой ткани и в настоящее время используется для диагностики ожирения, при котором ИМТ (вне беременности) составляет≥30 кг/м2 [1]. Жировая ткань является активным эндокринным органом. При избытке жировой ткани повышается уровень лептина и снижается уровень адипонектина, что приводит к инсулинорезистентности (ИР). Ожирение также часто ассоциировано с гиперандрогенемией. Эти и другие разнообразные гормональные изменения становятся причиной ановуляции [2].
До сих пор не совсем ясно, ожирение само по себе является фактором увеличения риска неблагоприятных исходов беременности или предрасполагает к развитию других патологических состояний, повышающих эти риски [3]. Неблагоприятные исходы беременности часто связывают с нарушениями углеводного обмена, которые выявляются у значительной части женщин с ожирением. Однако у женщин с ожирением и нормальной толерантностью к глюкозе вероятность осложненного течения беременности остается повышенной [4]. Считается, что в патогенез вовлечены различные механизмы дизрегуляции метаболических, сосудистых и провоспалительных эффектов жировой ткани в отношении других органов и систем [5]. Это предположение поддерживает тот факт, что частота некоторых осложнений беременности увеличивается по мере прогрессирования ожирения [1,2, 6].
Эпигенетические изменения в ответ на повышенные концентрации глюкозы, липидов и провоспалительных цитокинов, внутриутробно воздействующие на плод, могут привести к транзиторным или перманентным изменениям метаболического программирования, и это будет проявляться повышенным риском различных заболеваний в течение всей последующей жизни [7].
Распространенность ожирения среди женщин репродуктивного возраста широко варьирует в зависимости от использованного критерия, года исследования и особенности изучаемой популяции, однако четко отмечается увеличение доли этих женщин в соответствии с ростом распространенности ожирения в общей популяции [8]. По данным исследования NHANES (National Health and Nutrition Examination Survey), проведенного в 2011–2012гг., доля страдающих ожирением в возрасте от 20 до 39 лет составила 31% (ИМТ ≥30 кг/м2); наибольшая распространенность была среди афроамериканок (56,6%) [9]. Для сравнения: в 1980 г. (до рутинного использования ИМТ) только у 7% женщин на первом пренатальном визите отмечалась масса тела более 95 кг [10].
Влияние на фертильность. Ожирение часто ассоциировано с синдромом поликистозных яичников (СПКЯ), который характеризуется ановуляцией. При СПКЯ одним из основных патогенетических механизмов является ИР. Считается, что ответная гиперинсулинемия нарушает нормальный фолликулогенез. Восстановление овуляции, наблюдающееся у женщин с СПКЯ на фоне снижения массы тела и лечения метформином, поддерживает эту концепцию [11, 12]. Однако даже при отсутствии СПКЯ у женщин с ожирением имеются проблемы фертильности. Время до наступления беременности увеличивается пропорционально увеличению массы тела [13].
Неблагоприятные факторы, связанные с ожирением, повреждают овариальную функцию и снижают качество ооцитов, кроме того, возможны тонкие отрицательные воздействия на рецепторный аппарат эндометрия. Некоторые наблюдательные исследования продемонстрировали, что потеря веса приводит к благоприятным гормональным изменениям и улучшению фертильности у женщин с ожирением [14, 15]. Необходимы большие рандомизированные исследования, чтобы подтвердить эти предварительные выводы.
Эффективность лечения бесплодия при помощи вспомогательных репродуктивных технологий (ВРТ). У женщин с ожирением риск неудач в ходе лечения бесплодия при помощи ВРТ выше по сравнению с женщинами с нормальной массой тела. В ряде исследований снижение эффективности лечения бесплодия было ассоциировано с более низким количеством и качеством полученных ооцитов, а также с низким качеством эмбрионов [16, 17]. В других исследованиях было показано, что при сравнимых показателях частоты наступления клинической беременности и живорожденных детей женщинам с ожирением требуются более высокие дозы гонадотропинов для стимуляции овуляции по сравнению с женщинами с нормальной массой тела [18, 19]. В систематическом обзоре и метаанализе 33 исследований, включавших почти 48 тыс. лечебных циклов экстракорпорального оплодотворения (ЭКО) / ИКСИ (от англ. ICSI — IntraCytoplasmic Sperm Injection, букв. введение сперматозоида в цитоплазму, интрацитоплазматическая инъекция сперматозоида) с использованием собственных ооцитов, у женщин с ИМТ ≥25 кг/м2 по сравнению с женщинами с ИМТ 4 кг и длина >54 см к моменту рождения)). Многие исследования показали линейную корреляцию между ИМТ матери до беременности и весом новорожденного [3, 51, 53]; таким образом, у матерей с ожирением отмечается более высокая частота макросомии [1, 2, 10, 29, 41]. Эта взаимосвязь не зависит от частоты ГСД у женщин с ожирением [4, 51, 53].
У макросомии есть 2 потенциальных осложнения: дистоция плечиков и более высокая предрасположенность к развитию ожирения в дальнейшей жизни. Данные проспективных когортных исследований показали, что при нормализации массы тела у женщины с ожирением снижается риск рождения крупного плода [58, 59]. В популяционных когортных исследованиях было продемонстрировано, что у женщин с исходным ожирением, снизившим ИМТ на 2 кг/м2 перед зачатием, снижается риск рождения крупного ребенка по сравнению с женщинами, которые поддерживают высокий ИМТ (ОР 0,61, 95% ДИ 0,52–0,73) [59].
Аутизм и другие расстройства психического развития детей. В популяционном исследовании методом «случай – контроль» была выявлена ассоциация между ИР матери и частотой аутизма и других расстройств психического развития детей [54]. Это наблюдение требует дальнейших подтверждений.
Астма у детей. В недавнем метаанализе обсервационных исследований была показана взаимосвязь между ожирением матери и повышением риска астмы и бронхообструктивного синдрома у детей (ОР 1,35, 95% ДИ 1,08–1,68; 5 исследований); наличие астмы в анамнезе матери не влияло на эти показатели [55]. Возможные биологические механизмы могут активизировать провоспалительные и иммунологические факторы.
Тактика прегравидарной подготовки женщин с ожирением. Курация женщин с ожирением, планирующих беременность, должна проводиться с позиций мультидисциплинарного подхода, и команда специалистов должна включать терапевта, акушера-гинеколога, эндокринолога, диетолога, психотерапевта и, возможно, других специалистов. Перед зачатием пациентке с ожирением необходимо провести обследование для исключения эндокринных расстройств (гипотиреоза, синдрома поликистозных яичников, гиперкортицизма и др.). Помимо негативного влияния на репродуктивную функцию ожирение может приводить к кардиоваскулярным и цереброваскулярным заболеваниям, СД 2-го типа, синдрому апноэ сна, остеоартритам и некоторым видам рака. Поэтому обследование может включать и другие исследования.
Тактика прегравидарной подготовки женщин с ожирением должна включать:
•компенсацию/устранение эндокринных расстройств (если таковые имеются);
•улучшение чувствительности к инсулину (при диагностированных нарушениях углеводного обмена);
•снижение массы тела;
•поддержку лютеиновой фазы препаратами прогестерона.
Снижение массы тела на этапе планирования беременности необходимо для оптимизации репродуктивной функции и улучшения исходов беременностей у женщин с ожирением [3, 56–60], хотя положительно сказывается и на общесоматическом здоровье. Достижение идеальной массы тела не всегда оказывается реальной целью лечения. Для восстановления регулярной менструальной̆ функции и овуляции, а также для снижения рисков осложнений беременности в большинстве случаев достаточно снизить массу тела на 10—15% от исходной, или уменьшить ИМТ на 2–5 кг/м2 от начальных параметров [61].
Первой рекомендацией при ожирении являются изменение образа питания, более подвижный образ жизни и модификация поведенческих реакций. Ни одна из диет не показала значимых преимуществ в эффективности снижения массы тела, поэтому главным является уменьшение объема потребляемой пищи и увеличение физических нагрузок [62]. Если в течение 3-х мес. на фоне изменения образа жизни не достигнуто снижение веса на 5% от исходной массы тела, инициируется медикаментозная терапия [1–3].
Современные руководства по лечению ожирения акцентируют: у пациентов с избыточной массой тела или ожирением, уже имеющих ассоциированные сопутствующие заболевания, медикаментозная терапия должна начинаться одновременно с модификацией образа жизни [62]. Дисфункцию яичников, бесплодие, гиперандрогению можно полноправно считать расстройствами, ассоциированными с ожирением. Таким образом, при ИМТ ≥ 25 кг/м2 у женщины с нарушениями менструальной и/или репродуктивной функции оправданно назначение препаратов для снижения массы тела вместе с рекомендациями по изменению образа жизни. Практически все препараты для медикаментозного лечения ожирения не используются во время беременности и применяются только на этапе прегравидарной подготовки.
В Российской Федерации для долгосрочного применения с целью снижения массы тела одобрены орлистат (ингибитор липазы) и сибутрамин (ингибитор обратного захвата моноаминов) [63].
Рандомизированные исследования показали, что снижение массы тела на фоне приема орлистата было на 2% больше, чем на фоне приема плацебо [64]. Систематический обзор и метаанализ 45 исследований с вовлечением 7788 участников показали более выраженное снижение массы тела на фоне модификации образа жизни и применения орлистата в течение 12 мес. по сравнению с изменением образа жизни без приема препарата: среднее снижение массы тела составило 1,8 и 1,56 кг соответственно [64]. Так как препарат препятствует всасыванию жиров, фармакологический эффект зависит от наличия жиров в рационе питания. Пациенткам, принимающим орлистат, рекомендуется диета с их низким содержанием для повышения эффективности лечения и минимизации побочных эффектов. Основные побочные эффекты включают стеаторею, метеоризм, императивные позывы на дефекацию.
В ходе рандомизированных исследований было отмечено, что на фоне применения сибутрамина масса тела снижается на 5% больше, чем на фоне приема плацебо. Комбинация приема сибутрамина с изменением стиля жизни показала наилучшие результаты по сравнению с монотерапией сибутрамином или изменениями стиля жизни и питания – через 12 мес. лечения снижение массы тела составило 12,1 5,0, и 6,7 кг соответственно [65]. Побочные эффекты сибутрамина включают повышение артериального давления и тахикардию за счет адренергических свойств препарата, поэтому сибутрамин противопоказан при сердечно-сосудистых заболеваниях и стойкой артериальной гипертензии. К сожалению, назначение сибутрамина без учета противопоказаний в ходе крупного исследования SCOUT привело к увеличению числа нефатальных инфарктов миокарда и нефатальных инсультов у пациентов с кардиоваскулярными заболеваниями, принимающих сибутрамин [66], что вызвало сомнения в его безопасности. Тщательный пересмотр полученных данных позволил сделать заключение, что при отсутствии сердечно-сосудистых заболеваний препарат является эффективным и безопасным средством для снижения массы тела [67–69]. Предикторами повышения риска сердечно-сосудистых заболеваний на фоне применения сибутрамина явились отсутствие снижения массы тела[68] и, наоборот, быстрое значительное снижение массы тела и АД у пациентов старше 55 лет [69].
Систематический обзор нескольких схем лечения ожирения – а именно сибутрамин 10 мг, сибутрамин 15мг, орлистат 120 мг или римонабант 10 мг по сравнению с изменением образа жизни и/или плацебо – по результатам 94 исследований с участием 24 808 пациентов продемонстрировал, что сибутрамин 15 мг имеет наилучший фармакоэкономический профиль по сравнению с другими схемами лечения [70].
В Российской Федерации сибутрамин входит в состав препарата Редуксин, который дополнительно содержит микрокристаллическую целлюлозу. Эффективность и безопасность данного препарата были оценены в многоцентровых наблюдательных программах «Весна» и «ПримаВера», которые проходили на базе ведущих медицинских учреждений во всех регионам РФ [71–73]. В рамках программы «ПримаВера» было подтверждено положительное влияние Редуксина на динамику веса пациентов, зафиксировано отсутствие серьезных рисков проводимого лечения и серьезных нежелательных эффектов при назначении препарата с учетом противопоказаний [72, 73]. Всего в исследовании «ПримаВера» приняли участие 98774 больных с ожирением.
Для того чтобы оценить эффективность Редуксина в снижении массы тела у женщин репродуктивного возраста, для анализа была выделена группа женщин в возрасте от 18 до 40 лет (средний возраст – 30,3±5,3 года), в которую вошли 2578 участниц. Было показано, что через 12 мес. лечения у 94% пациенток репродуктивного возраста масса тела снизилась более чем на 10% от исходной: у 41% пациенток – на 11–20%, у 53% – >20%. ИМТ нормализовался у 25,5% пациенток, а доля женщин с ИМТ ≥35 кг/м2 снизилась с 40,3 до 2,5%. Объем талии пациенток уменьшился со 103 до 85см, что говорит об уменьшении абдоминального ожирения. Побочные эффекты не отмечались в 95,3% случаев, что подчеркивает безопасность препарата при его правильном назначении. Таким образом, сочетание сибутрамина с микрокристаллической целлюлозой является эффективным и безопасным средством для снижения массы тела у пациенток репродуктивного возраста с ожирением.
Заключение. Ожирение у женщин репродуктивного возраста ассоциировано с рядом общесоматических и репродуктивных проблем, что приводит к снижению фертильности. Жировая ткань является местом периферического синтеза многих гормонов, а также активно участвует в работе сосудистой системы и формировании иммунного ответа, поэтому ее избыточное содержание сопровождается метаболическими, гормональными, сосудистыми и провоспалительными нарушениями. У женщин с ожирением по сравнению с женщинами с нормальной массой тела снижена как частота наступления спонтанных беременностей, так и эффективность лечения бесплодия различными методами (стимуляция овуляции, ВРТ). После наступления беременности у женщин с ожирением повышены риски врожденных аномалий плода, макросомии, мертворождения, гестационной гипертензии, гестационного сахарного диабета, преждевременных родов и ряда других осложнений. Снижение массы тела положительно влияет на менструальную функцию, повышает вероятность зачатия и рождения здорового ребенка, уменьшает риск неблагоприятных исходов беременности. Приемлемым параметром снижения массы тела на этапе прегравидарной подготовки является 10% от исходной массы тела, особенно в случаях выраженного ожирения. Сибутрамин в сочетании с микрокристаллической целлюлозой является эффективным и безопасным препаратом для снижения массы тела у женщин репродуктивного возраста.
студент, кафедра медицинской биохимии НГМУ
РФ, г. Новосибирск
д-р мед. наук, профессор, кафедра медицинской биохимии НГМУ,
РФ, г. Новосибирск

Ожирение – избыточное накопление жировой ткани в организме, характеризующееся нарушением липидного и углеводного обмена с последующими патологическими изменениями [6]. В настоящее время это заболевание является одним из самых социально значимых хронических заболеваний, которое принимает масштабы эпидемии.
Ожирение развивается, когда количество поступившей энергии в организм превышает ее расход, такое ожирение называют алиментарным. Также существует и эндокринное ожирение, но оно составляет лишь 5% от всех случаев, обычно, люди с таким ожирением имеют характерные внешние признаки, которые позволяют опознать и предупредить дальнейшее развитие заболевания.
Для того чтобы определить каким видом ожирения страдает пациент необходимо провести обследование: измерить рост и вес (для вычисления ИМТ), окружность талии и бедер; измерить АД; провести биохимический анализ крови для установления уровня глюкозы и мочевой кислоты; определить липидный спектр; из гормональных исследований – необходимо проверить уровень ТТГ [7].
В настоящее время известно две основные группы гормонов, которые участвуют в регуляции пищевого поведения: оказывающие орексиогенный эффект (увеличивающие потребление пищи) и обладающие анорексиогенным действием (уменьшающие потребление пищи). Наиболее важные из них: лептин, грелин и серотонин.
Лептин секретируются адипоцитами (жировой тканью), слизистой дна желудка, скелетными мышцами, а также эпителием молочных желез и плацентой. Этот гормон отвечает за подавление чувства голода и секрецию инсулина, вызывает инсулинорезистентность скелетных мышц и жировой ткани, усиливает термогенез.
Грелин отвечает за появление чувства голода. Вырабатываясь в желудке и тонком кишечнике, он поступает в кровоток. Перед приемом пищи в крови возрастает уровень этого гормона, и, воздействуя на клетки гипоталамуса, грелин возбуждает чувство голода.
Содержащийся в энтерохромаффинных клетках кишечника, ЦНС (в гипоталамусе и среднем мозге), тромбоцитах серотонин, при снижении концентрации, приводит к усилению аппетита, алкоголизму, табакокурению, наркомании, токсикомании, депрессии и утрате контроля над поведением[4]. При нарушении соотношения этих гормонов формируется атипичное пищевое поведение, что приводит к избыточному потреблению пищи, и как следствие возникает ожирение.
С избыточным весом связано многократное повышение риска и частоты развития артериальной гипертонии, инсулиннезависимого сахарного диабета, атеросклероза и ишемической болезни сердца. Но особое внимание следует уделить этому заболеванию в связи с тем, что оно сопровождается метаболическими нарушениями и патологическим функционированием репродуктивной системы, что может привести к тяжелому течению беременности, преждевременным родам и развитием осложнений у потомства[6].
Во время беременности создаются благоприятные условия для развития жировой клетчатки, которая служит метаболической защитой будущему ребенку. С первых дней беременности в организме женщины происходят гормональные изменения: повышается синтез прогестерона, хорионического гонадотропина, пролактина и плацентарного лактогена. Все эти гормоны стимулируют отложение в организме жировой ткани [3].
На характер распределения жировой ткани в организме влияют гормоны половых желез и надпочечников, но особо важна роль конверсии андрогенов в эстрогены, которая осуществляется в адипоцитах. Во время беременности повышается продукция и инактивация андрогенов, так как повышается скорость их метаболического клиренса, это способствует поддержанию нормального соотношения уровней андрогенов, циркулирующих в крови. Но у 20-50% женщин с ожирением может наблюдаться значительное повышение уровня андрогенов (тестостерона, дегидроэпиандростерона, дегидроэпиандростерон – сульфата), вследствие чего развивается гиперандрогения, которая может привести к невынашиванию беременности [3].
В последние годы было обнаружено, что плацента человека секретирует лептин, адипонектин, резистин и рецепторы к ним. Эти адипоцитокины способны модулировать пролиферацию и инвазию трофобласта, а также влиять на процессы ангиогенеза. Беременность приводит к метаболическим изменениям, тем самым влияя на ее течение. На ранних сроках (первые 12 недель) концентрация лептина в крови увеличивается на 30% и выше. Но у пациентов с ожирением наблюдается другой профиль этого гормона: уровень лептина в сыворотке крови матери пропорционален увеличению ее веса с самого начала беременности (уровень значительно превышает норму).
Адипонектин также играет огромную роль в развитии патогенеза ожирения. В ходе беременности секреция гормона в белой жировой ткани снижается на 60%, но так как плацента способна синтезировать этот гормон, то на 24 неделе его концентрация повышается более чем в 20 раз.
Резистин – пептидный гормон, его также называют адипоцит — специфичным фактором. В каждом организме он секретируется моноцитами, макрофагами и адипоцитами. Этот гормон в естественных условиях снижает толерантность к глюкозе, вызывая резистентность к инсулину (по данным исследования на грызунах). В плаценте человека резистин синтезируется клетками трофобласта, и с увеличением срока беременности, уровень гормона также возрастает[5].
Наиболее распространенные осложнения, в которых не последнюю роль играют описанные выше гормоны, являются гестационный сахарный диабет (ГСД) и преэкплампсия (ПЭ).
Гестационный сахарный диабет (ГСД) – это сахарный диабет (СД) любой этиологии, а также нарушение толерантности к глюкозе, которое возникло и выявлено во время беременности. На развитие этого заболевания влияет множество факторов: этническое происхождение, возраст и семейный анамнез, но его частота увеличивается в 2-3 раза у лиц с избыточной массой тела по сравнению с женщинами, которые имеют нормальный вес. Ожирение и инсулинорезистентность изменяют функцию плаценты, что приводит к увеличению поступления глюкозы, аминокислот и жирных кислот к плоду. Гипергликемия матери вызывает и гипергликемию у плода, которая сопровожается гипертрофией/гиперплазией поджелудочной железы плода, вследствие чего возникает гиперинсулинемия. Высокий уровень инсулина в крови плода влияет на деление его клеток, что ведет к развитию макросомии. Данное проявление фенопатии плода увеличивает риски тяжелых родов и материнских/неонатальных осложнений. При ГСД также увеличивается концентрация ФНО и ИЛ-6 (провоспалительные цитокины), вызывая воспаление, они стимулируют секрецию лептина, который самостоятельно может повышать уровень ФНО и ИЛ-6, вследствие этого развивается порочный круг воспалительных процессов.
Преэклампсия (ПЭ) – осложнение беременности, которое характеризуется развитием гипертонии и протеинурии. В среднем это осложнение встречается у 2-5% беременных и является основной причиной перинатальной, неонатальной и материнской заболеваемости и смертности. Как и ГСД, ПЭ ассоциирована с факторами риска, такими как, резистентность к инсулину, субклиническое воспаление и ожирение. У женщин с этим заболеванием повышен риск развития сердечно – сосудистых заболеваний. Также наблюдается высокий риск гипертонии, ишемической болезни сердца, инсульта и венозной тромбоэмболии.
Одним из инициаторов ПЭ является снижение перфузионного давления матки, а нарушение плацентации и дисбаланс между ангиогенезом и антиангиогенными факторами являются основными причинами развития ПЭ. На развитие и исход ПЭ немаловажную роль играют гормоны жировой ткани, в частности лептин. Увеличение концентрации этого гормона на каждые 10 нг/мл увеличивает риск ПЭ на 30%. Также при ПЭ увеличивается уровень адипонектина на 30-87%, который может ослаблять чрезмерную воспалительную реакцию в сосудистой стенке. Роль резистина в развитии ГСД и ПЭ противоречива, но его концентрация в крови увеличена у женщин с ожирением[3].
Кроме этих осложнений у 43% женщин с ожирением еще до наступления беременности диагностируется артериальная гипертензия, которая является одним из факторов риска развития ПЭ. Частота истмико – цервикальной недостаточности у беременных с избыточной массой тела выше, чем у женщин с нормальным ИМТ [2]. Также у пациенток с ожирением выявляется ранний токсикоз, угроза прерывания беременности встречается в 1,5 раза чаще, анемия в 4 раза, бессимптомная бактериурия в 5 раз. У них также дагностируется метаболический синдром (гипертринглицеридемя, снижение образования ЛПВП, микроальбуминурия, гиперинсулинемия), а выделительная функция почек (снижение выделения креатинина и появление микроальбуминурии) снижается[1].
Чтобы избежать нежелательных последствий избыточного веса для матери и ее ребенка, необходимо заняться его профилактикой до беременности и в период самой беременности. Для этого нужно контролировать массу тела и различные метаболические нарушения, сбалансировано питаться и адекватно соблюдать физические нагрузки[3].
Список литературы:
- Боровкова Е.И., Байрамова М.Ю. Течение беременности и родов у пациенток с ожирением Макаров И.О. // Акушерство, гинекология и репродукция. -2011. — Т.5. — №1. — С. 22-28.
- Колосова Т.А. Беременность и роды у женщин с ожирением дефицитом массы тела: диссертация на соискание ученой степени кандидата медицинских наук / ГОУВПО «Российский университет дружбы народов». – М., 2012. – С. 8-10.
- Комшилова К.А., Дзгоева Ф.Х. Беременность и ожирение // Ожирение и метаболизм. — 2009. — №4. — С. 9-13.
- Мищенкова Т.В., Звенигородская Л.А. Роль гормонов и типов пищевого поведения в развитии абдоминального ожирения, методы лечения ожирения // Вестник эстетической медицины. — 2010. — Т.9. — №4. — С. 37-43.
- Петунина Н.А., Кузина И.А. Роль гормонов жировой ткани в развитии осложнений беременности у женщин с ожирением // Ожирение и метаболизм. -2013. — №1 (34). — С.3-8.
- Тагиева Ф.А. Ожирение и репродуктивное здоровье женщины // Актуальные проблемы частной медицины: Вестник украинской медицинской академии. – 2016. — Т.16. — №2 (54). — С. 317-320
- Шведова А.Е. Ожирение: что это такое и как с ним бороться // Ожирение и метаболизм. — 2007. — №2. — С. 42-45.

В современном мире ожирение является одной из самых распространенных форм нарушений жирового обмена, причем частота данной патологии не имеет тенденции к снижению, число беременных с ожирением достигает 15,5-26,9% [1, с. 5–7; 2, с. 56; 3, с. 9–11]. Заболеваемость ожирением во всем мире уже достигла масштабов эпидемии и, по прогнозам некоторых ученых, вырастет до 70% к 2025 году [4, с. 18]. Данные литературы и акушерской практики свидетельствуют о том, что ожирение значительно осложняет течение беременности и родового акта, способствуя возникновению акушерских осложнений в 2-3 раза чаще, чем у женщин, имеющих обычную массу тела.
Цель исследования: изучить течение беременности и родов у женщин с ожирением. Выявить связь осложнений со степенью ожирения. Сравнить полученные данные с данными литературы.
Методы: исследование зависимости осложнений беременности и родов от степени ожирения путем корреляционного анализа, графическое представление результатов.
Место проведения: Мордовский республиканский клинический перинатальный центр.
Источник данных: проанализированы истории родов 99 женщин, родоразрешенных в Мордовском республиканском клиническом перинатальном центре в период с 1 сентября по 31 декабря 2017 года.
Клинические группы: все женщины были разделены на 3 клинические группы в соответствии со степенью ожирения. 1 группу составили женщины с ИМТ от 30,0 до 34,9, то есть с І степенью ожирения; 2 группа — женщины со ІІ степенью ожирения, ИМТ составляет 35,0–39,9; 3 клиническая группа соответствует ІІІ степени ожирения, ИМТ >40,0.
В зарубежных источниках избыток массы тела, как правило, оценивают по индексу массы тела (ИМТ) или по индексу Кетле. Вычисляется он по формуле: масса тела (кг) / рост в квадрате (м) [5, с. 9–13].
Существует классификация массы тела по ИМТ Международной группы по ожирению (IOFT):
- недостаточная масса тела составляет 40,0 [6, с. 28].
Медико-социальная характеристика клинических групп: в 1 группу вошло 33 женщины, средний возраст которых составляет 25 лет. Из них 29 женщин находится в браке, 30 работающих, 2 студентки. Средняя прибавка массы тела за время беременности 13 кг.
Во 2 клиническую группу вошло 33 женщины со средним возрастом 29 лет. В браке находится 27 женщин, 28 работающих. Средняя прибавка массы тела во время беременности 11 кг.
3 клиническая группа состоит из 33 женщин, их средний возраст составляет 30 лет. Из них 25 женщин состоит в браке, 27 работающих. Средняя прибавка массы тела за время беременности составила 11 кг.
Установлено, что существует связь ожирения матери и функции внешнего дыхания ребенка как в период новорожденности, детства, так и в зрелом возрасте. Ожирение матери приводит к повышению окислительного стресса в маточно-плацентарно-плодовом комплексе, что оказывает влияние на состояние ДНК, белков и липидов во всех трех структурах. Дисбаланс окислительно-восстановительных реакций, ведущий к оксидативному стрессу в период беременности, связан и с другими осложнениями, в том числе преэклампсией (до 10,2%), РДС и повреждением легких после рождения.
Одними из самых распространенных осложнений, связанных с материнским лишним весом, являются преждевременный разрыв плодных оболочек, что составляет от 10 до 40%, преждевременная отслойка нормально расположенной плаценты (до 2%), врожденные аномалии плода, мертворождение (риск увеличивается в 2 раза по сравнению с беременными, имеющими нормальную массу тела), перенашивание встречается в 10-20% случаев, ограничение роста плода, преждевременные роды и кесарево сечение (5-10%) [7, с. 248].
В ходе проведенных исследований были выявлены следующие распространенные осложнения: угроза преждевременных родов была диагностирована у 21 женщины в 1 клинической группе, что составило 64% от общего числа, в 23 случаях у женщин из 2 группы, что равняется 70%, и у 24 женщин в 3 клинической группе, что составляет 73% (рис. 1).
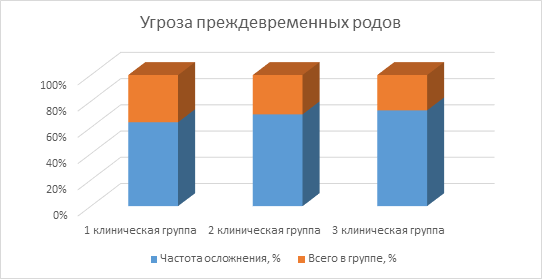
Рис. 1. Угроза преждевременных родов
Частота родоразрешения путем операции кесарево сечение составила 18 случаев в 1 клинической группе, 22 случая во 2 группе, 27 случаев отмечалось в 3 клинической группе. Таким образом, наибольшая частота данного осложнения наблюдалась в 3 клинической группе, что составило 82% от общего числа женщин, тем самым доказывая, что чем больше ожирение, тем выше частота операции кесарево сечение (рис. 2).
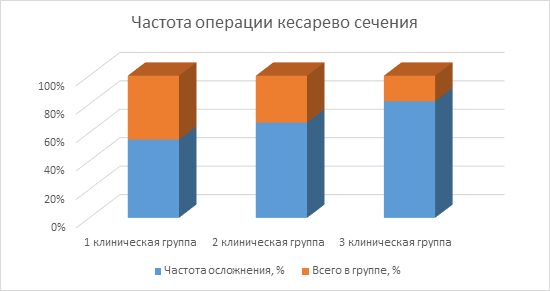
Рис. 2. Частота операции кесарево сечение
Преждевременный разрыв плодных оболочек зарегистрирован у 14 женщин в 1 клинической группе, в 15 случаях во 2 группе и в 19 клинических случаях в 3 группе, что отражает связь со степенью ожирения (рис. 3).
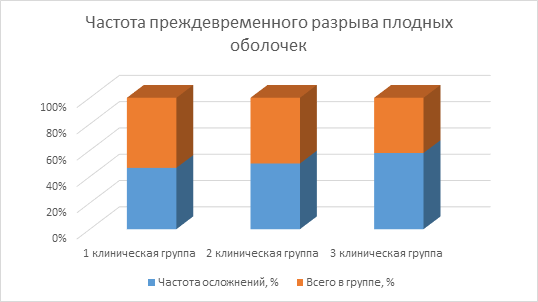
Рис. 3. Частота преждевременного разрыва плодных оболочек
При оценке состояния новорожденных было отмечено, что в 6 клинических случаях были рождены недоношенные дети, из них 1 случай в 1 клинической группе, 2 случая во 2 группе и 3 случая в 3 группе. Наблюдались 2 случая рождения крупного к сроку гестации плода в 3 клинической группе. Врожденные аномалии имелись у 1 беременной из 3 клинической группы, ее масса тела составляла 142 кг на момент родов. ВПС у плода проявлялся в виде тетрады Фалло. Умеренный комбинированный стеноз легочной артерии с умеренной гипоплазией ствола и ветвей легочной артерии. Установлено, что смертность в течение первого года жизни составляет 25%, к 3 годам — 40%, к 10 годам — 70% и к 40 годам смертность достигает 95%. Обычно тяжелые неоперированные пациенты умирают от тромбоэмболии в сосуды головного мозга с образованием абсцессов, сердечной недостаточности, инфекционного эндокардита [8].
При оценке новорожденного по системе Апгар на 1 минуте жизни средний показатель составил 8 баллов в 1 группе, 8 баллов во 2 группе и 7 баллов в 3 клинической группе. При оценке через 5 минут средний показатель составил 8 баллов в 3 исследуемых группах.
Материнское ожирение связано с повышением инсулинорезистентности на протяжении всей беременности по сравнению с женщинами нормального веса, что приводит к увеличению плацент-опосредованного транспорта глюкозы к плоду [9, с. 145-148]. Кроме того, увеличение резистентности к инсулину у женщин с ожирением увеличивает риск гестационного диабета, который в свою очередь изменяет глюкокортикоид-опосредованное развитие легких плода в конце беременности и тормозит созревание сурфактанта, что приводит к повышенному риску развития РДС при рождении [7, с. 248]. В ходе проведенного исследования было выявлено 14 случаев гестационного сахарного диабета, что составляет 14% от общего числа исследуемых.
По данным некоторых авторов, ожирение может изменить материнскую HPA ось и привести к повышенному количеству кортизола у плода. Длительное пребывание плода в избытке глюкокортикоидов является ключевым механизмом, который влияет на развитие его организма. В частности, регуляция материнской гипоталамо-гипофизарно-надпочечниковой (HPA) оси определяет воздействие гормонов стресса на плод, влияние фетального программирования HPA оси, а также течение и исход родов. Во время нормальной беременности материнская HPA ось претерпевает существенные изменения, связанные с увеличением концентрации кортизола в три раза выше нормального уровня к третьему триместру. Плод частично защищен от высокого уровня материнских глюкокортикоидов действием фермента 11β-гидроксистероиддегидрогеназы-2, который экспрессируется в плаценте. Этот фермент действует на преобразование кортизола в своей неактивной форме в кортизон, тем самым защищая плод от чрезмерного воздействия глюкокортикоидов. Хотя значительная часть кортизола превращается в кортизон плацентой, избыток кортизола может достигать плода в случаях нарушения функции плаценты, например в результате материнского стресса, инфекции или воспаления. Ожирение может влиять на плацентарный транспорт жирных кислот, что приводит к увеличению движущей силы диффузии через плаценту, нарушению развития плаценты, а также изменению площади поверхности для обмена. Это приводит к увеличению проникновения липидов через плаценту, в результате чего возникает дислипидемия и накопление жира у плода.
Известно, что частой патологией послеродового периода у родильниц с избыточной массой тела являются кровотечения, встречающиеся у 6-30% женщин, что в 2-5 раз превышает аналогичные показатели у родильниц с нормальной массой тела [6, с. 249]. В исследуемых группах данная патология не была выявлена. Послеродовый период у родильниц с ожирением достаточно часто сопровождается осложнениями инфекционного и неинфекционного характера. Так, эндометрит развивается в 2,6-17% случаев, субинволюция матки – в 35%, лохиометра – в 12-14%, тромбофлебит – в 8-21,5%; в целом различные послеродовые осложнения у женщин с ожирением отмечаются в 47-53% случаев [6, с. 249]. При анализе исследуемой группы послеродовый эндометрит был выявлен в 6 случаях, что составляет 6% от общего числа обследованных. Это, по-видимому, связано с проведением своевременной профилактики послеродовых гнойно-септических осложнений, путем назначения антибактериальной терапии [10, с. 115].
Согласно полученным данным, общее число осложнений в течение беременности и родов у женщин с ожирением выше, чем у женщин, имеющих нормальную массу тела. Все женщины были разделены на 3 клинические группы в соответствии со степенью ожирения. В ходе проведенных исследований были выявлено, что такие осложнения, как угроза преждевременных родов, преждевременный разрыв плодных оболочек, чаще встречаются у женщин из 3 клинической группы, то есть ИМТ>40,0. Частота родоразрешения путем операции кесарево сечение составила 18 случаев в 1 клинической группе, 22 случая во 2 группе, 27 случаев отмечалось в 3 клинической группе, тем самым доказывая, что чем больше ИМТ, тем выше частота операции кесарево сечение. При оценке состояния новорожденных было выявлено, что чем выше степень ожирения беременной женщины, тем ниже баллы по системе Апгар у новорожденных. Таким образом, выявляется прямолинейная корреляционная связь между осложнениями беременности и родов и степенью ожирения.
Несмотря на наличие большого количества осложнений, ожирение не является противопоказанием к беременности. При подготовке к зачатию женщине необходимо провести прегравидарную подготовку не только у врача акушера-гинеколога, но и у эндокринолога. Согласно ВОЗ, оптимальный ИМТ должен составлять от 18 до 24, 9 кг/м2. ИМТ от 25 до 29,9 считают как избыток массы тела, от 30 — как ожирение. Рекомендовано обучение таких пациенток в «Школе для больных ожирением». Таким образом, беременная может получить информацию о гестационных рисках, обусловленных ожирением, неблагоприятном влиянии на плод соматических заболеваний. В преконцепционный период важно направить мероприятия на снижение массы тела: диетотерапия, оптимальный режим физических нагрузок, коррекция эндокринных нарушений и медикаментозная терапия ожирения [11, с. 33].
Во время беременности женщина должна руководствоваться определенными правилами: вынашивание беременности должно сопровождаться строгим контролем общей массы тела и прибавкой во время беременности, которая не должна превышать 5-6 кг. Соблюдение правильного питания: для того чтобы снизить возбудимость пищевого центра, рекомендуется частый прием пищи (6-8 раз в сутки). Пища должна быть низкокалорийной, но при этом занимать большой объем в желудке, что способствует устранению чувства голода. Рекомендуются такие закуски, как крекеры, сушеные фрукты и йогурты. Из рациона беременной необходимо исключить вкусовые вещества, способствующие повышению возбудимости пищевого центра и усиливающие аппетит. Содержание белка в рационе беременной должно составлять 20% от суточного рациона, доля жиров примерно 30%, а углеводов — 50%. Энергетическая ценность рациона должна в среднем составлять 2500 ккал в сутки. Важно понимать, что беременной нельзя голодать, так как это может привести к развитию кетонемии. Беременным женщинам рекомендуется вести график результатов систематического взвешивания [12, с. 68].


